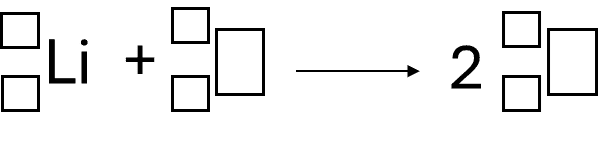
Wszystkie zadania
Zadanie 3
Temperatura krzepnięcia roztworów jest niższa niż temperatura krzepnięcia czystego rozpuszczalnika. Im więcej drobin wprowadzi się do danej masy rozpuszczalnika, tym niższą temperaturę krzepnięcia ma otrzymany roztwór. Zjawisko obniżenia temperatury krzepnięcia w odniesieniu do temperatury krzepnięcia czystego rozpuszczalnika nazywamy efektem krioskopowym.W dwóch zlewkach (oznaczonych jako I i II)znajdowało się po 500 g wody. Następnie do każdej wprowadzono odpowiednią ilość substancji:
Zlewka I – 0,5 mol glukozy
Zlewka II – 0,5 mol sacharozy
Zlewka III – 0,5 mol chlorku sodu
Zlewka IV – 0,5 mol siarczanu(VI) baru
Zawartość każdej zlewki zamieszano. W każdej stwierdzono obecność fazy ciekłej.Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli informacja jest fałszywa.
Roztwór w zlewce II ma niższą temperaturę krzepnięcia niż roztwór w zlewce I, ponieważ sacharoza jest dwucukrem budowanym z glukozy i fruktozy. P F Ciecz w zlewce III ma taką samą temperaturę krzepnięcia, jak ciecz w zlewce IV P F W jednym naczyniu w praktyce nie zaobserwowano efektu krioskopowego P F Zadanie 4
Przeprowadzono dwuetapowe doświadczenie. Pierwszy etap przedstawiono poniżej:
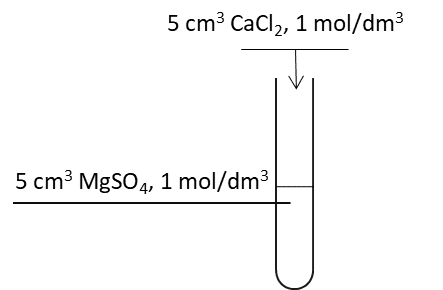
Zaobserwowano powstanie białego osadu. Zawiesinę przesączono. W etapie II do 5 cm3 przesączu dodano 5 cm3 roztworu BaCl2 o stężeniu 1 mol/dm3.
Napisz równanie reakcji zachodzącej w etapie II lub napisz, że reakcja nie zachodzi.
Zadanie 6
Kwas cytrynowy jest kwasem trójprotonowym. Z przesyconych roztworów kwasu cytrynowego (C6H8O7) w wodzie wypadają kryształy o wzorze C6H8O7·xH2O. W celu ustalenia współczynnika x próbkę kryształów o masie 1,211 g (otrzymanych z wodnego roztworu) rozpuszczono w wodzie i miareczkowano roztworem NaOH w obecności fenoloftaleiny. Do pojawienia się trwałego różowego zabarwienia zużyto 69,2 cm3 roztworu NaOH o stężeniu 0,2500 mol/dm3.
Zadanie 6.1
Oblicz wartość współczynnika x.Zadanie 6.2
Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli informacja jest fałszywa.
W opisanym hydracie kwasu cytrynowego na jedną cząsteczkę kwasu przypada jedna cząsteczkę wody, a w hydracie o wzorze CuSO4·5H2O na jedną cząsteczkę soli przypada pięć cząsteczek wody. P F Rozpuszczenie w wodzie bezwodnego kwasu cytrynowego i pozostawienie do odparowania wody prowadzi do otrzymania kryształów o wzorze C6H8O7·H2O P F Kwas cytrynowy może reagować z NaOH w stosunku molowym nkwasu : nNaOH = 1 : 1. P F Znanych jest wiele syntetycznych radioizotopów niklu. Część z nich o niższych liczbach masowych ulega rzadziej obserwowanym typom rozpadów. Jądra atomowe niklu-48 rozpadają się wg różnych ścieżek, które zachodzą w tym samym czasie.
Zadanie 1
Jednym z produktów jest żelazo-46 oraz cząstki oznaczone umownie symbolem X.
Ustal symbol cząstki X i napisz równanie opisanej przemiany. Uzupełnij wszystkie pola w poniższym schemacie.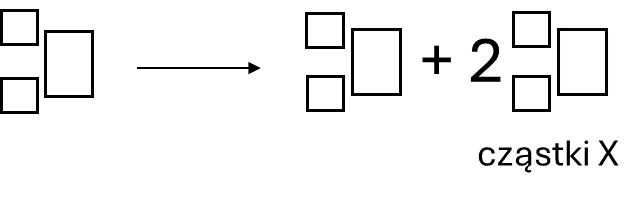
Zadanie 2
Kiedy jądro ma nadmiar protonów, w jego wnętrzu może zajść przemiana β+, w której z protonu powstają neutron, pozyton (e+ lub β+) i neutrino (ν).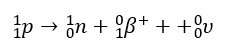
Pozyton jest cząstką różniącą się od elektronu tylko znakiem ładunku elektrycznego. Bezwzględna wartość ładunku oraz masa obydwu cząstek są jednakowe. Neutrino jest nienaładowaną elektrycznie cząstką o masie spoczynkowej bliskiej zeru.
Część jąder atomowych niklu-48 ulega rozpadowi w przemianie β+.
Napisz równanie opisanej przemiany. Uzupełnij wszystkie pola w poniższym schemacie.
Zadanie 3
Jądra atomowe trzeciego nuklidu, który powstaje w wyniku rozpadu niklu-48 ma liczbę masową równą 47. Podczas tego rozpadu emitowane są zarówno cząstki oznaczone jako X, jak i cząstki β+.
Ustal, które cząstki (cząstki oznaczone w zadaniu nr 1 jako X, cząstki β+) i w jakiej liczbie są emitowane podczas opisanej przemiany. Uzupełnij schemat, podaj symbol chemiczny oraz liczbę atomową powstającego nuklidu.Liczba cząstek X: …….
Liczba cząstek β+: …….
Atomy pewnego metalicznego pierwiastka oznaczonego umownie symbolem X występują naturalnie w postaci 5 izotopów o liczbach masowych: 58 (68,077% atomów), 60 (26,233% atomów), 61 (1,14% atomów), 62 (3,634% atomów) oraz 64 (0,926%).
W wyniku analizy pewnej próbki metalu X stwierdzono, że średnia ważona liczb masowych wszystkich atomów jest równa 59,142.
Zadanie 1
Wykonaj odpowiednie obliczenia i rozstrzygnij, czy analizowana próbka jest naturalnie występującą mieszaniną izotopów, czy też jest sztucznie wzbogacona w jeden z izotopów.Rozstrzygnięcie: ……………………….
Zadanie 2
Z podanego zestawu wybierz tę wartość, która przedstawia masę atomową naturalnego pierwiastka X. Podaj jego symbol.
a) 57,935 u
b) 58,693 u
c) 58,766 u
d) 59,142 u
e) 59,452 u
Symbol pierwiastka: ……….Tlenek wapnia w sposób egzotermiczny reaguje z wodą wg równania:
CaO + H2O → Ca(OH)2
Przeprowadzono dwa doświadczenia, przedstawione na schemacie. Wszystkie składniki oraz otoczenie miały początkową temperaturę 25 °C. Temperatura otoczenia nie zmieniła się podczas doświadczenia.
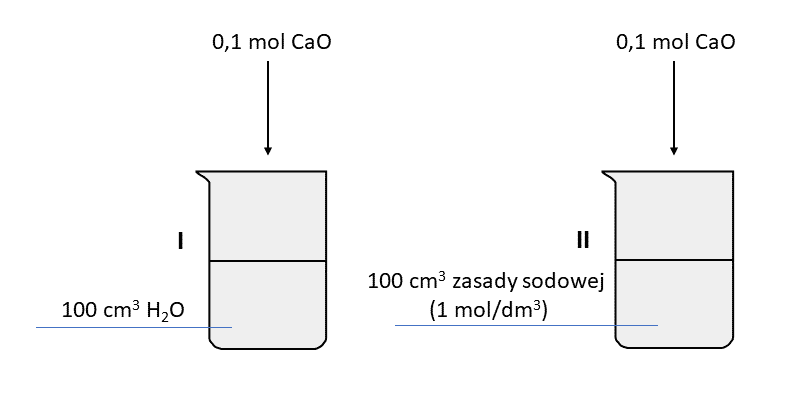
Zadanie 1
Uzupełnij zdania. Wybierz i podkreśl po jednym określeniu z nawiasu.
Po zamieszaniu zawartości temperatura układu w zlewce I była (wyższa od 25 °C / niższa od 25 °C), co oznacza, że układ (zaczął oddawać ciepło do otoczenia / przyjmować ciepło od otoczenia). Po zakończeniu zmian w zlewce I otrzymano (układ jednorodny / zawiesinę).Zadanie 2
W zlewce II zaobserwowano powstanie zawiesiny.
Wybierz zdanie, które w prawidłowo opisuje wynik doświadczenia w zlewce II.
A. W zlewce II nie doszło do zmiany temperatury, ponieważ tlenek wapnia nie reaguje z zasadą sodową.
B. Otrzymanie zawiesiny świadczy o tym, że tlenek wapnia nie reaguje z zasadą sodową.
C. W zlewce II zaszła reakcja, ale jej substraty i produkty są inne niż w zlewce I, więc efekt cieplny jest inny niż w zlewce I. Powstanie zawiesiny nie świadczy o braku reakcji w zlewce II.
D. Tlenek wapnia przereagował z zasadą sodową, a efekt cieplny jest praktycznie taki sam jak w zlewce I. Powstanie zawiesiny nie świadczy o braku reakcji w zlewce II.
Nie uwzględniając izomerii optycznej, wyróżniamy 4 alkohole o wzorze C4H9OH (butylowe). Wszystkie w stanie ciekłym są bezbarwnymi cieczami, ale różnią się właściwościami fizycznymi. W tabeli przedstawiono wzory odpowiednich izomerów i temperatury przemian fazowych pod ciśnieniem 1013 hPa.
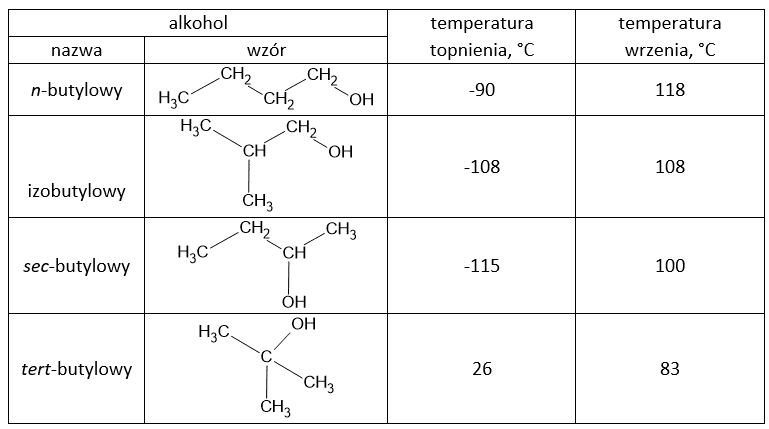
Zadanie 1
W szafce laboratoryjnej przechowywana jest erlenmajerka z jednym z izomerów. Erlenmajerkę po wyjęciu z szafki przedstawiono na fotografii.
Rozstrzygnij, który z alkoholi butylowych jest przechowywany w erlenmajerce. Podaj jego nazwę zwyczajową lub systematyczną. Uzasadnij swój wybór.
Nazwa: …………………………………………………..
Uzasadnienie:..................................................................................
Zadanie 2
Rozstrzygnij, czy zdanie poniżej jest prawdziwe, czy fałszywe. Wybierz i podkreśl jedno określenia z nawiasu i uzasadnij swój wybór.
Z podanych alkoholi najmniej lotny jest alkohol tert-butylowy, ponieważ ma najwyższą temperaturę topnienia.
Rozstrzygnięcie: zdanie jest (prawdziwe / fałszywe).
Uzasadnienie: .......................................................Prezentowane zadanie jest autorską propozycją jak mogłoby wyglądać zadanie nr 17 z arkusza maturalnego z 16.05.2024. Propozycja ta wynika z dyskusyjnego zachowania styrenu (w oryginalnym zadaniu 17) w prezentowanych warunkach. W tej propozycji styren zastąpiono cykloheksyloetenem.
Zadanie 17
Cykloalkany ulegają analogicznym reakcjom jak alkany.
Benzen, cykloheksan i winylocykloheksan to węglowodory, które w temperaturze pokojowej są bezbarwnymi cieczami. Ich wzory przedstawiono poniżej:
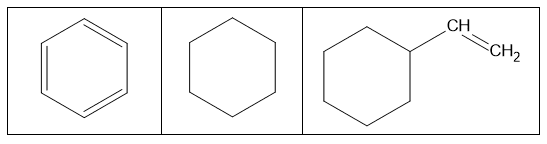
W trzech naczyniach znajdowały się oddzielnie i w przypadkowej kolejności: benzen, cykloheksan i winylocykloheksan. W celu identyfikacji tych substancji wykonano dwuetapowe doświadczenie. W pierwszym etapie do trzech probówek zawierających wodny roztwór manganianu(VII) potasu w środowisku obojętnym wprowadzono po jednej z badanych substancji. Następnie każdą probówkę zamknięto korkiem i wstrząśnięto. Po pewnym czasie zawartości probówek przybrały wygląd pokazany na zdjęciach.

W pierwszym etapie zidentyfikowano jeden z trzech węglowodorów. W drugim etapie doświadczenia do próbek niezidentyfikowanych węglowodorów wprowadzono stężony kwas azotowy(V) z dodatkiem stężonego kwasu siarkowego(VI) – i ogrzano zawartości probówek. Wyniki drugiego etapu doświadczenia przedstawiono na poniższych zdjęciach.
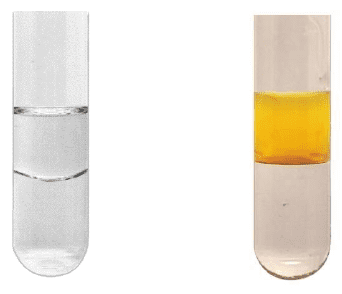
Zadanie 17.1
Napisz wzór sumaryczny związku manganu, który powstał w wyniku reakcji zachodzącej w pierwszym etapie doświadczenia, oraz wzór półstrukturalny (grupowy) lub uproszczony organicznego produktu tej przemiany.
Zadanie 17.2
Napisz równanie reakcji, która umożliwiła odróżnienie związków w drugim etapie doświadczenia.
..........................................
Zadanie to jest autorską propozycją jak mogłoby wyglądać zadanie nr 27 z arkusza maturalnego z 16.05.2024 (F2023), aby było ono jednoznaczne
i zgodnie z właściwościami chemicznymi przedstawionych substancji.Przeprowadzono reakcje zgodnie ze schematem:
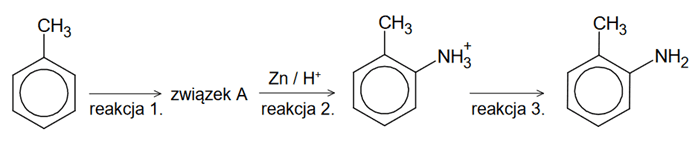
Do organicznego związku w reakcji 1. wkraplano brom w obecności światła. Wkraplanie przerwano, gdy osiągnięto stosunek molowy substancji 1 : 1.
Zadanie 27
Narysuj wzór półstrukturalny lub uproszczony organicznego produktu opisanej reakcji i uzupełnij zdanie. Wybierz i zaznacz właściwą odpowiedź spośród podanych w nawiasie.
Opisana przemiana (jest / nie jest) reakcją utlenienia-redukcji.
Komentarz autora: informacja do zadania w oryginalnym brzmieniu mówi o produkcie reakcji 3 (2-metyloaniliny) i jego dalszej reakcji z bromem. Niestety, ale obecność grupy -NH2 związanej z pierścieniem aromatycznym silnie aktywuje pierścień w reakcjach substytucji elektrofilowe (anilina w reakcji z wodą bromową daje prawie natychmiast osad 2,4,6-tribromoaniliny - bez żadnych katalizatorów). Z tego też powodu zmieszanie z bromem może doprowadzić do bardzo gwałtownej reakcji (a nawet wybuchu) po zmieszaniu reagentów i bez udziału światła. Finalnym produktem powinna być 2,4-dibromo-6-metyloanilina, a w przypadku stosunku molowego 1 : 1 mieszanina 2,4-dibromo-6-metyloaniliny, 2-bromo-6-metyloaniliny i 4-bromo-6-metyloaniliny. Grupa -NO2 jest podstawnikiem bardzo silnie dezaktywujacym pierścień aromatyczny - po zmieszaniu w bromem reakcja powinna zajść dopiero przy naświetlaniu, analogicznie jak w przypadku bromowania toluenu na świetle. Związek taki pojawia się jako związek A (produkt reakcji 1).