Wszystkie zadania
W dwóch pojemnikach o stałej objętości 2 dm3 znajdowały się gazy o temperaturze 20 °C i pod ciśnieniem 1013 hPa. W pierwszym: azot, w drugim: amoniak. Następnie do każdego naczynia wpompowano po 1 dm3 ciekłej wody o tej samej temperaturze. Otrzymano układ jak na przedstawionym obrazku.
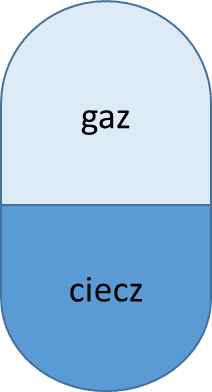
Po pewnym czasie dokonano pomiaru ciśnienia w obu zbiornikach. Stwierdzono, że w jednym zbiorniku ciśnienie jest blisko 2 razy wyższe od 1013 hPa, a w drugim – spadło znacznie poniżej 1013 hPa, podczas gdy temperatura w obu zbiornikach nie uległa zmianie względem pierwotnej wartości.
Zadanie 1
Napisz, jaki gaz był zawarty w zbiorniku, w którym zaobserwowano znaczny spadek ciśnienia. Uzasadnij swój wybór.Zadanie 2
Tylko w jednym ze zbiorników zaobserwowano wielokrotny wzrost przewodnictwa elektrycznego fazy ciekłej. Napisz równanie równowagowego procesu odpowiedzialnego ten fakt.Zadanie 2
Kwas ortofosforowy(V) o wzorze H3PO4 jest ostatecznym i trwałym produktem uwodnienia dekatlenku tetrafosforu. Znanych jest jednak wiele kwasów fosforowych i ich soli. Kwasy takie są produktami częściowego uwodnienia dekatlenku tetrafosforu. Kwas difosforowy(V), zwany także pirofosforowym(V) ma wzór H4P2O7.Związek ten rozpuszczony w wodzie jest kwasem Broensteda, a ujemne logarytmy poszczególnych stałych równowagi dysocjacji (w 25 °C) mają następujące wartości: pKa1 = 0,91, pKa2 = 2,10, pKa3 = 6,70, pKa4 = 9,32.
Zadanie 2.1
Oceń poprawność zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli jest fałszywa.H4P2O7 jest kwasem słabszym od H3PO4
P
F
H4P2O7 jest kwasem czteroprotonowym
P
F
Zadanie 2.2
Difosforany(V) można otrzymać w wyniku ogrzewania wodorofosforanów(V), np.: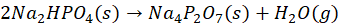
Difosforan(V) sodu jak i kwas disfosforowy są dobrze rozpuszczalne w wodzie. Cechą charakterystyczną takich roztworów jest ich nietrwałość. W roztworach tych dochodzi do powolnej reakcji z wodą, o czym świadczą zmiany pH tych roztworów (pomiary wykonywane w tej samej temperaturze).
a) Napisz w postaci cząsteczkowej równanie reakcji kwasu difosforowego(V) z wodą.
b) Napisz w postaci jonowej równanie reakcji anionów difosforanowych(V) z wodą.
Zadanie R1
Przygotowano zestaw 2 probówek, w których (w nieznanej kolejności) umieszczono roztwór wodorosiarczanu(IV) sodu w wodzie oraz roztwór siarczanu(IV) sodu w wodzie.Do obu probówek wprowadzoną po kilka kropel roztworu KMnO4. Zanotowano następujące zmiany:
I – powstanie brunatnej zawiesiny, po opadnięciu osadu ciecz nad nim jest bezbarwna
II – powstanie bezbarwnego roztworu
Napisz wzory soli, które znajdowały się w poszczególnych probówkach.
Probówka I:…………………………………………………..
Probówka II:………………………………………………….
W celu oznaczenia udziału (w % masowych) NH4NO3 w nawozie zawierającym wyłącznie NH4NO3 i KNO3, próbkę o masie 2,000 g rozpuszczono w wodzie i wprowadzono do roztworu z nadmiarem KOH. Zaszła wtedy reakcja chemiczna opisana równaniem:
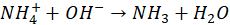
Z roztworu poreakcyjnego usunięto cały amoniak, który następnie pochłonięto w płuczce zawierającej 50 cm3 wodnego roztworu H2SO4 o stężeniu 0,1000 mol/dm3. Nadmiar H2SO4 został odmiareczkowany roztworem NaOH o stężeniu 0,1000 mol/dm3. Do osiągnięcia punktu końcowego zużyto 75,0 cm3 roztworu NaOH.
Oblicz, jaki jest udział masowy NH4NO3 w badanym nawozie sztucznym. Wynik podaj w %.
O cząsteczce pewnego węglowodoru wiadomo, że jej wzór spełnia warunek CnH2n+2. Jednocześnie wiadomo, że poszczególnym atomom węgla łańcucha głównego tej cząsteczki ponumerowanym od 1 do 5 można przypisać stopień utlenienia:
lokant
1
2
3
4
5
typ hybrydyzacji
-III
-I
-I
-II
-III
Wiadomo też, że w cząsteczce tego węglowodoru można wyróżnić 4 grupy metylowe.
Napisz nazwę systematyczną tego węglowodoru.
Nazwa:……………………………………………
O cząsteczce pewnego węglowodoru wiadomo, że jej wzór spełnia warunek CnH2n. Jednocześnie wiadomo, że poszczególnym atomom węgla w tej cząsteczce ponumerowanym od 1 do 5 można przypisać typ hybrydyzacji:
lokant
1
2
3
4
5
typ hybrydyzacji
sp3
sp3
sp3
sp3
sp3
Napisz nazwę systematyczną tego węglowodoru i podaj liczbę wiązań typu p w jego cząsteczce.
Nazwa:……………………………………………
Liczba wiązań typu π:…………………….