Wszystkie zadania
Zadanie R6
Siarczan(IV) amonu jest solą dobrze rozpuszczalną w wodzie. Ze względu na podatność anionu na utlenianie – roztwory takie nie są trwałe, jeśli są wystawione na działanie powietrza. Odczyn roztworu siarczanu(IV) amonu można jednoznacznie potwierdzić za pomocą błękitu bromotymolowego.Zadanie R6.1
Na podstawie odpowiednich danych ustal odczyn wodnego roztworu siarczanu(IV) amonu w temperaturze 25 °C. Napisz, jaką barwę przyjmie błękit bromotymolowy w roztworze tej soli.Odczyn: ……………………………
Barwa wskaźnika: …………………………Zadanie R6.2
Do probówki wprowadzono 5 cm3 wodnego roztworu siarczanu(IV) amonu o stężeniu 0,2 mol/dm3 i dodano kilka kropel roztworu wskaźnika. Następnie wprowadzono 1 cm3 roztworu nadtlenku wodoru o stężeniu 1 mol/dm3.
Napisz w formie jonowej skróconej równanie reakcji utleniania, która zaszła po wprowadzeniu roztworu nadtlenku wodoru. Podaj barwę roztworu po zakończeniu reakcji chemicznej.Równanie reakcji utleniania: ……………………………………
Barwa wskaźnika po zakończeniu reakcji chemicznej: …………………………………………….
Zadanie R7
Anilina to najważniejsza amina aromatyczna. Główną metodą produkcji aniliny jest to redukcja nitrobenzenu. Najstarszą przemysłową metodą produkcji aniliny jest tak zwany proces Bechampa. Poniżej przedstawiono schemat reakcji zachodzącej podczas tego procesu:
C6H5NO2 + Fe + H2O → C6H5NH2 + Fe3O4
a) Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji redukcji oraz równanie reakcji utleniania zachodzących podczas opisanej przemiany. Uwzględnij, że proces biegnie w obecności katalitycznych ilości kwasu solnego.równanie redukcji: .................................................................
równanie utleniania: ..............................................................
b) Uzupełnij współczynniki stechiometryczne w poniższym schemacie.
....C6H5NO2 + ....Fe + ....H2O → ....C6H5NH2 + ....Fe3O4
Poniżej przedstawiono wartości iloczynu jonowego wody w zakresie temperatury 0 °C - 100 °C (pod ciśnieniem atmosferycznym).

We wrzącej wodzie rozpuszczono nieznaczną ilość pewnej soli i utrzymywano stałą temperaturę roztworu (100 °C). W tej temperaturze dokonano pomiaru pH roztworu. Otrzymano wartość pH równą 7,00.
Z podanych poniżej wzorów soli.
NH4Cl, CH3COONa, KCl
wybierz tę, która mogła być wprowadzona do wody, podaj jej nazwę i uzasadnij swój wybór.Nazwa soli: ................................
Uzasadnienie: ................................................
Zadanie 5
Poniżej podano efekty energetyczne dwóch reakcji jonowych w stanie standardowym:NaOH(aq) + HCl(aq) → NaCl(aq) + H2O + 55,8 kJ
Ba(NO3)2(aq) + Na2SO4(aq)→ BaSO4(s) + 2NaNO3(aq) + 26,3 kJ
Przeprowadź obliczenia i na podstawie powyższych danych oszacuj standardową entalpię reakcji o podanym równaniu:
Ba(OH)2(aq) + H2SO4(aq) → BaSO4(s) + 2H2O(c)
W celu otrzymania propanalu zaplanowano przeprowadzić reakcję, którą opisuje równanie stechiometryczne:
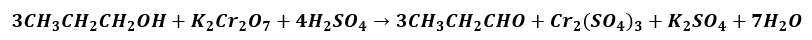
W metodzie tej stosuje się wodny zakwaszony roztwór K2Cr2O7. Ze względu na podatność aldehydu na dalsze utlenianie do kwasu karboksylowego stosuje się nadmiar alkoholu. Z mieszaniny poreakcyjnej łatwo wydzielić aldehyd metodą destylacji, więc reakcję przeprowadza się w odpowiedniej aparaturze. Jeden z odczynników podawany jest z wkraplacza po kropli do kolby reakcyjnej, w której znajduje się mieszany drugi odczynnik. Napisz, który zestaw jest prawidłowo zaplanowany, by wydajność otrzymywania aldehydu była jak najwyższa? Uzasadnij swój wybór.
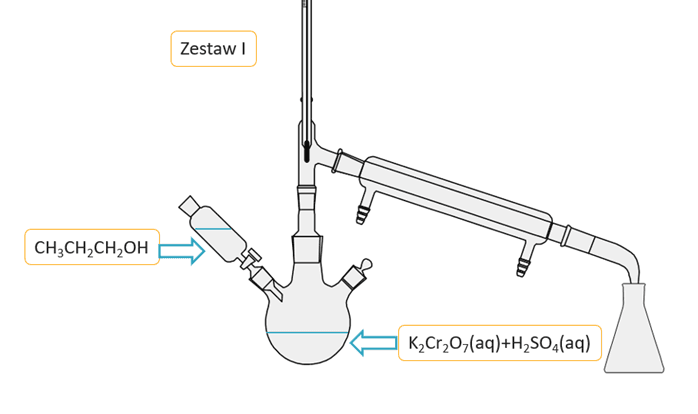
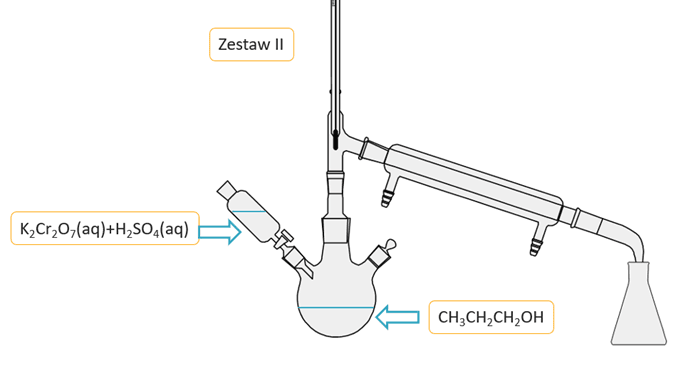
Zestaw:........
Uzasadnienie:...........
Zadanie R5
Po zmieszaniu wodnego roztworu azotanu(V) srebra(I) z wodnym roztworem nadtlenodisiarczanu potasu dochodzi do wytrącenia brunatnoczarnego osadu. Schemat reakcji przedstawiono poniżej.
AgNO3 + K2S2O8 + H2O → Ag4O4 + KHSO4 + HNO3
Zadanie R5.1
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie.
Równanie redukcji:………………..
Równanie utleniania:……………..
Zadanie R5.2
Związek o wzorze Ag4O4 ma bardzo silne właściwości utleniające. Potraktowany stężonym kwasem azotowym roztwarza się tworząc roztwór o intensywnej barwie brunatnej. W roztworze tym srebro istnieje w postaci dwudodatnich kationów. Po rozcieńczeniu tego roztworu w wodzie ponownie strąca się Ag4O4.
Napisz w postaci cząsteczkowej równanie reakcji zachodzącej po wprowadzeniu stałego Ag4O4 do stężonego kwasu azotowego(V) (równanie I) oraz po rozcieńczeniu otrzymanego roztworu w wodzie (równanie II).Równanie I: ………………..
Równanie II: …………….....
Zadanie R5.3
Na podstawie przedstawionych informacji określ trwałość kationów srebra w wodnym środowisku w zależności od stopnia utlenienia. Dokończ zdania. Wybierz i podkreśl jedną z odpowiedzi z podanych w nawiasach.
Kationy Ag+ są (trwałe / nietrwałe) w wodnym środowisku.
Kationy Ag2+ są (trwałe / nietrwałe) w wodnym środowisku.
Zadanie R3.1
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie.KHSO4(aq) + F2 (g) ⟶ K2S2O8(aq) + HF(aq)
Równanie redukcji:………………..
Równanie utleniania:……………..Zadanie R3.2
Napisz w formie jonowej skróconej sumaryczne równanie reakcji utleniania i redukcji
…………………………………………………………………………………….
Zadanie R3.3
Rozstrzygnij poprawność twierdzenia. Wybierz jedno określenie z podanych w nawiasie i uzasadnij wybór.
Anion siarczanowy(VI) nie może pełnić roli reduktora, ponieważ zawiera atom siarki na najwyższym możliwym stopniu utlenienia.
Twierdzenie (jest prawdziwe / nie jest prawdziwe), ponieważ…..
Zadanie R4
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie. Napisz w formie jonowej skróconej sumaryczne równanie reakcji utleniania i redukcji.
a) S2O32- + I2 → S4O62- + I-
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___S2O32- + ___I2 → ___S4O62- + ___I-
b) Ag4O4 + Sn2+ + H+ → Ag + Sn4+ + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Ag4O4 + ___Sn2+ + ___H+ → ___Ag + ___Sn4+ + ___H2O
c) PbO2 + Mn2+ + H+ → Pb2+ + MnO4- + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___PbO2 + ___Mn2+ + ___H+ → ___Pb2+ + ___MnO4- + ___H2O
d) Zn + NO3- + H+→ Zn2+ + NH3OH+ + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Zn + ___NO3- + ___H+→ ___Zn2+ + ___NH3OH+ + ___H2O
e) Cu2O + [Ag(NH3)2]+ + H2O → [Cu(NH3)4]2+ + Cu(OH)2 + Ag
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Cu2O + ___[Ag(NH3)2]+ + ___H2O → ___[Cu(NH3)4]2+ + ___Cu(OH)2 + ___Ag
f) [Cr(OH)6]3- + [Ag(NH3)2]+ + OH- → CrO42- + Ag + NH3 + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___[Cr(OH)6]3- + ___[Ag(NH3)2]+ + ___2OH- → ___CrO42- + ___Ag + ___NH3 + ___H2O
Zadanie R2
Kwas cytrynowy (kwas 2-hydroksypropano-1,2,3-trikarboksylowy) poddany działaniu wodnego roztworu KMnO4 ulega reakcji, w której zostaje przekształcony w kwas acetono-1,3-dikarboksylowy. Jednocześnie obserwuje się powstanie brunatnej zawiesiny i uwalnianie bezbarwnego gazu. Ciało stałe usuwa wprowadzając roztwór szczawianu amonu oraz rozcieńczony roztwór H2SO4 w wodzie. Na końcu, do bezbarwnego roztworu wprowadza się wodę bromową – powoduje to strącenie praktycznie nierozpuszczalnego w wodzie pentabromoacetonu i wydzielenie bezbarwnego gazu.Napisz w formie jonowej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy), równanie reakcji redukcji i równanie reakcji utleniania, które zaszły podczas opisanej przemiany. Uwzględnij środowisko reakcji. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
a) Po dodaniu roztworu KMnO4 do roztworu kwasu cytrynowego.
Równanie redukcji: …………………………………………………………………………………
Równanie utleniania: .......................................................................................................
b) Po wprowadzeniu roztworu szczawianu amonu i roztworu H2SO4.
Równanie redukcji: ………………………………………………………………………………………..
Równanie utleniania:
c) Po wprowadzeniu wody bromowej.Równanie redukcji: ………………………………………………………………………………………..
Równanie utleniania:
Zadanie 2
Mieszaniu cieczy towarzyszy zjawisko kontrakcji objętości, czyli zmiana objętości układu. np. w temperaturze pokojowej po wprowadzeniu do jednego naczynia 100 cm3 etanolu i 100 cm3 czystej wody otrzymuje się ok. 194 cm3 roztworu, zamiast spodziewanych 200 cm3.
Wyjaśnij, dlaczego zjawiska zmniejszenia objętości układu nie obserwuje się po umieszczeniu w jednym naczyniu 100 cm3 n-heksanu i 100 cm3 czystej wody.