Zadania z działu: Stechiometria
Omówienie tego zadania znajdziesz w lekcji LIVE w kursie Rozpuszczalność i hydraty
W celu określenia składu hydratu wodorotlenku baru wykonano następującą analizę. Odważono 2,970 g hydratu i rozpuszczono w wodzie otrzymując 100,0 cm3 roztworu. Następnie pobierano po 25 cm3 tego roztworu i w obecności błękitu bromotymolowego, przy ciągłym mieszaniu za, wkraplano (miareczkowano) wodny roztwór HCl o stężeniu 0,200 mol·dm–3 aż do zmiany barwy wskaźnika na zieloną. W trzech miareczkowaniach na każde zobojętnienie 25,0 cm3 roztworu wodorotlenku baru zużyto kolejno: 23,5 cm3, 23,6 cm3 i 23,6 cm3 kwasu solnego.
Ustal wzór analizowanego hydratu wodorotlenku baru. Wpisz brakujący współczynnik stechiometryczny w podanym wzorze. W obliczeniach zastosuj średnią objętość kwasu solnego zużytą w pojedynczym miareczkowaniu.Wzór hydratu: Ba(OH)2·……….H2O
Soda oczyszczona NaHCO3 i soda kalcynowana Na2CO3 są dodatkami do żywności określanymi jako E500 - węglany sodu. Trzecim dodatkiem z grupy węglanów sodu jest soda śnieżna Na3H(CO3)2 (wodorodiwęglan sodu). Sodę kalcynowaną otrzymuje się w wyniku ogrzewania (kalcynacji) sody oczyszczonej lub sody śnieżnej.
Zadanie 1
Napisz równanie reakcji otrzymywania sody kalcynowanej z sody śnieżnej.
.............................Zadanie 2
Oblicz, ile sody kalcynowanej otrzymuje się w wyniku kalcynacji 1 tony sody śnieżnej aż do uzyskania stałej masy..............................
Poziom trudności: łatwy/średni
Ile bezwodnego siarczanu(VI) magnezu MgSO4 należy dodać do 200 g 20% wodnego roztworu tej soli, aby otrzymać MgSO4·7H2O? Wynik podaj z dokładnością do czterech cyfr znaczących.
Zadanie pochodzi z I części podręcznika "Podstawy obliczeń chemicznych" D. Mickiewicza, nr 7.96.Poziom trudności: średni
W reakcji 50,00 g kwasu salicylowego C7H6O3 z 200,00 g kwasu octowego C2H4O2 otrzymano 50,00 g czystej aspiryny C9H8O4, którą wydzielono metodą krystalizacji. Oblicz wydajność otrzymywania aspiryny tą metodą oraz stopień przereagowania w chwili przerwania reakcji, jeśli wiesz, że wydajność krystalizacji wynosi 92%. Wynik podaj w procentach z dokładnością do jedności.
Zadanie pochodzi z pierwszej części podręcznika „Podstawy obliczeń chemicznych”, nr 7.97
Poziom trudności: średni
Tlenek wapnia CaO reaguje z wodą wg równania:
CaO + H2O ⟶ Ca(OH)2
Ile CaO należy dodać do 1000 g wody, aby otrzymać mleko wapienne o zawartości 10% masowych Ca(OH)2? Wynik podaj w g w dokładnością do jednej dziesiątej. Wskazówka: rozbij proces na etap hydratacji oraz na proces mieszania wodorotlenku z wodą, możesz też przyjąć (ale nie musisz), że wodorotlenek wapnia jest hydratem tlenku wapnia CaO·H2O i licz tak, jakby to miało miejsce w przypadku hydratu.
Zadanie pochodzi z pierwszej części podręcznika „Podstawy obliczeń chemicznych”, nr 7.95.
Poziom trudności: trudne
Kwas cytrynowy C6H8O7 w wodnych roztworach jest kwasem trójprotonowym przez obecność trzech kwasowych grup COOH. Anion tego kwasu ma wzór sumaryczny C6H5O73-. Cytrynian wapnia jest trudno rozpuszczalny w wodzie – w temperaturze 25 ℃ w 1 kg wody rozpuszcza się zaledwie 0,950 g tego związku. Z wody wytrąca się lub krystalizuje w postaci tetrahydratu i w tej postaci został znaleziony jako minerał w osadach z dna morskiego w okolicach Antarktydy i nazwany na cześć odkrywcy Earlandytem. Ustal wzór sumaryczny tej soli w postaci Cax(C6H5O7)y. Oblicz, jaka będzie wydajność otrzymywania cytrynianu wapnia w postaci hydratu, zakładając, że jest nią masa osadu powstałego w reakcji 5% roztworu kwasu cytrynowego oraz 5% mleka wapiennego wymieszanych w stechiometrycznym stosunku w podanej temperaturze.
Zadanie pochodzi z pierwszej części podręcznika „Podstawy obliczeń chemicznych”, nr 7.104.
Poziom trudności: średni
Dwutlenek siarki otrzymuje się przez spalanie siarki w nadmiarze powietrza. Oblicz minimalną (stechiometryczną) objętość powietrza (m3 w warunkach normalnych) potrzebną na spalenie 1 tony siarki. Pamiętaj, że tlen stanowi 21% obj. powietrza, a wynik podaj z dokładnością do jedności.
Zadanie pochodzi z pierwszej części podręcznika „Podstawy obliczeń chemicznych”, nr 7.94.
Zadanie 6
Kwas cytrynowy jest kwasem trójprotonowym. Z przesyconych roztworów kwasu cytrynowego (C6H8O7) w wodzie wypadają kryształy o wzorze C6H8O7·xH2O. W celu ustalenia współczynnika x próbkę kryształów o masie 1,211 g (otrzymanych z wodnego roztworu) rozpuszczono w wodzie i miareczkowano roztworem NaOH w obecności fenoloftaleiny. Do pojawienia się trwałego różowego zabarwienia zużyto 69,2 cm3 roztworu NaOH o stężeniu 0,2500 mol/dm3.
Zadanie 6.1
Oblicz wartość współczynnika x.Zadanie 6.2
Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli informacja jest fałszywa.
W opisanym hydracie kwasu cytrynowego na jedną cząsteczkę kwasu przypada jedna cząsteczkę wody, a w hydracie o wzorze CuSO4·5H2O na jedną cząsteczkę soli przypada pięć cząsteczek wody. P F Rozpuszczenie w wodzie bezwodnego kwasu cytrynowego i pozostawienie do odparowania wody prowadzi do otrzymania kryształów o wzorze C6H8O7·H2O P F Kwas cytrynowy może reagować z NaOH w stosunku molowym nkwasu : nNaOH = 1 : 1. P F W wyniku całkowitego spalenia pary węglowodoru X otrzymano 7,5 dm3 (w przeliczeniu na warunki normalne) spalin zawierających tylko CO2 i H2O. Po wykropleniu pary wodnej pozostały gaz zajmuje w warunkach normalnych objętość 5 dm3. Gęstość par węglowodoru X jest 3 razy większa niż gęstość etynu (mierzona w identycznych warunkach).
Ustal nazwę węglowodoru X.W 20 °C rozpuszczalność Na2CO3 i NaHCO3 (w 100 g wody) wynosi odpowiednio 21,5 i 9,6 g. W temperaturze 20 °C przygotowano nasycony roztwór Na2CO3 przez rozpuszczenie 1 mola Na2CO3 w odpowiedniej ilości wody. Następnie, w zestawie uniemożliwiającym opuszczanie układ przez wodę na drodze parowania, przez roztwór przepuszczano gazowy CO2, aż przyrost masy zawartości naczynia wyniósł 44 g. Wydzielony krystaliczny osad odsączono i wysuszono. Wszystkie operacje wykonano nie zmieniając temperatury. Podczas przepuszczania CO2 przez roztwór zaszła reakcja, której równanie przedstawiono poniżej.
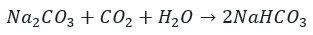
Zadanie 1
Oblicz wydajność otrzymywania NaHCO3 opisaną metodą. Załóż, że masa otrzymanego suchego NaHCO3 otrzymanego po odsączeniu i wysuszeniu ciała stałego jest równa masie wydzielonych kryształów. Przyjmij masy molowe: Na2CO3 – 106 g·mol-1, NaHCO3 – 84 g·mol-1, CO2 – 44 g·mol-1. Wynik podaj w procentach z dokładnością do jedności.Zadanie 2
Rozstrzygnij, czy prawdziwe jest poniższe stwierdzenie. Wybierz i podkreśl rozstrzygnięcie z podanych w nawiasie i uzasadnij swój wybór.
Twierdzenie: otrzymana masa kryształów świadczy o tym, że reakcja pomiędzy roztworem węglanu sodu a tlenkiem węgla(IV) zaszła w mniej niż 80%.
Twierdzenie (jest / nie jest) prawdziwe, ponieważ
……………………………………………………………………………………………………