Zadania z działu: Stechiometria
Sekcja laboratoryjna miała za zadanie otrzymać układy o odczynie obojętnym. W tym celu wykonano serię doświadczeń, których schematy przedstawiona na rysunku.
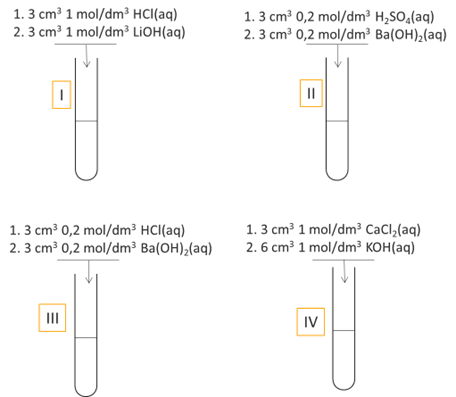
Wybierz numery wszystkich probówek, w których uniwersalny papierek wskaźnikowy zanurzony w mieszaninie poreakcyjnej wskaże odczyn obojętny.
Numery probówek……………………………………………………………………BaSO4 jest związkiem praktycznie nierozpuszczalnym w wodzie (0,0003 g/100 g wody w 25 °C). Strącono osad BaSO4 przez zmieszanie równych objętości roztworów BaCl2 i Na2SO4 o stężeniu 0,5 mol/dm3 w obu przypadkach. Objętość użytego roztworu BaCl2 wynosiła 0,25 dm3. Po opadnięciu osadu na dno ciecz zdekantowano, a osad zadano porcją 200 cm3 chemicznie czystej wody, zamieszano i ponownie zdekantowano. Płukanie osadu chemicznie czystą wodą wykonywano tak długo, aż w zdekantowanej cieczy nie obserwowano zmętnienia po zmieszaniu z wodnym roztworem AgNO3. Wtedy osad wysuszono. Stwierdzono, że jego masa wynosi 28,80 g.
Zadanie 1
Oblicz wydajność, z jaką otrzymano BaSO4 oraz masę NaCl w mieszaninie poreakcyjnej.
Zadanie 2
Podaj nazwę substancji odpowiedzialnej za zmętnienie powstające po zmieszaniu dekantowanej cieczy z roztworem AgNO3.Do odpowiednio przystosowanego naczynia zawierającego 100 g wody wrzucono 20 g potasu. Nastąpiła reakcja, podczas której uwalnia się ciepło, a faza stała uległa roztworzeniu. Podczas doświadczenia zbierano wodór, a na podstawie jego objętości stwierdzono, że otrzymano go z wydajnością 70%. Doświadczenie przeprowadzono tak, by woda ogrzana ciepłem reakcji nie opuszczała układu w postaci pary wodnej.
Oblicz stężenie procentowe otrzymanego roztworu oraz objętość zebranego wodoru (w warunkach normalnych).W celu oznaczenia udziału (w % masowych) NH4NO3 w nawozie zawierającym wyłącznie NH4NO3 i KNO3, próbkę o masie 2,000 g rozpuszczono w wodzie i wprowadzono do roztworu z nadmiarem KOH. Zaszła wtedy reakcja chemiczna opisana równaniem:
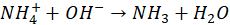
Z roztworu poreakcyjnego usunięto cały amoniak, który następnie pochłonięto w płuczce zawierającej 50 cm3 wodnego roztworu H2SO4 o stężeniu 0,1000 mol/dm3. Nadmiar H2SO4 został odmiareczkowany roztworem NaOH o stężeniu 0,1000 mol/dm3. Do osiągnięcia punktu końcowego zużyto 75,0 cm3 roztworu NaOH.
Oblicz, jaki jest udział masowy NH4NO3 w badanym nawozie sztucznym. Wynik podaj w %.