Zadania z działu: Chemia fizyczna
Poniżej przedstawiono wartości iloczynu jonowego wody w zakresie temperatury 0 °C - 100 °C (pod ciśnieniem atmosferycznym).

We wrzącej wodzie rozpuszczono nieznaczną ilość pewnej soli i utrzymywano stałą temperaturę roztworu (100 °C). W tej temperaturze dokonano pomiaru pH roztworu. Otrzymano wartość pH równą 7,00.
Z podanych poniżej wzorów soli.
NH4Cl, CH3COONa, KCl
wybierz tę, która mogła być wprowadzona do wody, podaj jej nazwę i uzasadnij swój wybór.Nazwa soli: ................................
Uzasadnienie: ................................................
Zadanie 5
Poniżej podano efekty energetyczne dwóch reakcji jonowych w stanie standardowym:NaOH(aq) + HCl(aq) → NaCl(aq) + H2O + 55,8 kJ
Ba(NO3)2(aq) + Na2SO4(aq)→ BaSO4(s) + 2NaNO3(aq) + 26,3 kJ
Przeprowadź obliczenia i na podstawie powyższych danych oszacuj standardową entalpię reakcji o podanym równaniu:
Ba(OH)2(aq) + H2SO4(aq) → BaSO4(s) + 2H2O(c)
W celu otrzymania propanalu zaplanowano przeprowadzić reakcję, którą opisuje równanie stechiometryczne:
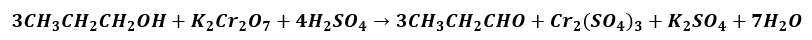
W metodzie tej stosuje się wodny zakwaszony roztwór K2Cr2O7. Ze względu na podatność aldehydu na dalsze utlenianie do kwasu karboksylowego stosuje się nadmiar alkoholu. Z mieszaniny poreakcyjnej łatwo wydzielić aldehyd metodą destylacji, więc reakcję przeprowadza się w odpowiedniej aparaturze. Jeden z odczynników podawany jest z wkraplacza po kropli do kolby reakcyjnej, w której znajduje się mieszany drugi odczynnik. Napisz, który zestaw jest prawidłowo zaplanowany, by wydajność otrzymywania aldehydu była jak najwyższa? Uzasadnij swój wybór.
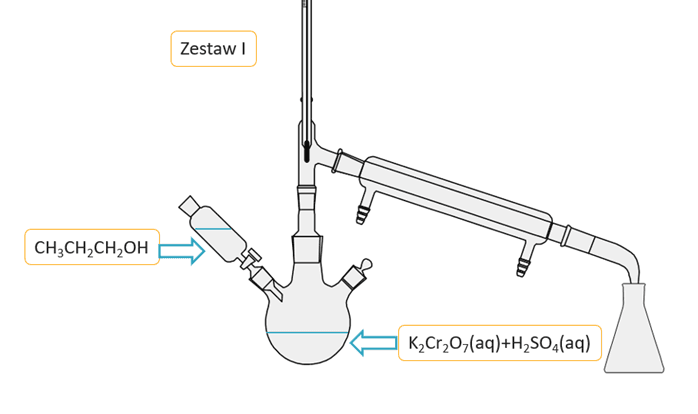
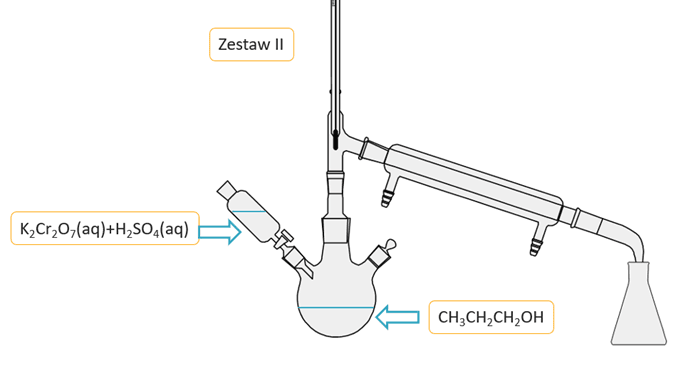
Zestaw:........
Uzasadnienie:...........
Zadanie R5
Po zmieszaniu wodnego roztworu azotanu(V) srebra(I) z wodnym roztworem nadtlenodisiarczanu potasu dochodzi do wytrącenia brunatnoczarnego osadu. Schemat reakcji przedstawiono poniżej.
AgNO3 + K2S2O8 + H2O → Ag4O4 + KHSO4 + HNO3
Zadanie R5.1
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie.
Równanie redukcji:………………..
Równanie utleniania:……………..
Zadanie R5.2
Związek o wzorze Ag4O4 ma bardzo silne właściwości utleniające. Potraktowany stężonym kwasem azotowym roztwarza się tworząc roztwór o intensywnej barwie brunatnej. W roztworze tym srebro istnieje w postaci dwudodatnich kationów. Po rozcieńczeniu tego roztworu w wodzie ponownie strąca się Ag4O4.
Napisz w postaci cząsteczkowej równanie reakcji zachodzącej po wprowadzeniu stałego Ag4O4 do stężonego kwasu azotowego(V) (równanie I) oraz po rozcieńczeniu otrzymanego roztworu w wodzie (równanie II).Równanie I: ………………..
Równanie II: …………….....
Zadanie R5.3
Na podstawie przedstawionych informacji określ trwałość kationów srebra w wodnym środowisku w zależności od stopnia utlenienia. Dokończ zdania. Wybierz i podkreśl jedną z odpowiedzi z podanych w nawiasach.
Kationy Ag+ są (trwałe / nietrwałe) w wodnym środowisku.
Kationy Ag2+ są (trwałe / nietrwałe) w wodnym środowisku.
Zadanie R3.1
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie.KHSO4(aq) + F2 (g) ⟶ K2S2O8(aq) + HF(aq)
Równanie redukcji:………………..
Równanie utleniania:……………..Zadanie R3.2
Napisz w formie jonowej skróconej sumaryczne równanie reakcji utleniania i redukcji
…………………………………………………………………………………….
Zadanie R3.3
Rozstrzygnij poprawność twierdzenia. Wybierz jedno określenie z podanych w nawiasie i uzasadnij wybór.
Anion siarczanowy(VI) nie może pełnić roli reduktora, ponieważ zawiera atom siarki na najwyższym możliwym stopniu utlenienia.
Twierdzenie (jest prawdziwe / nie jest prawdziwe), ponieważ…..
Zadanie R4
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie. Napisz w formie jonowej skróconej sumaryczne równanie reakcji utleniania i redukcji.
a) S2O32- + I2 → S4O62- + I-
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___S2O32- + ___I2 → ___S4O62- + ___I-
b) Ag4O4 + Sn2+ + H+ → Ag + Sn4+ + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Ag4O4 + ___Sn2+ + ___H+ → ___Ag + ___Sn4+ + ___H2O
c) PbO2 + Mn2+ + H+ → Pb2+ + MnO4- + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___PbO2 + ___Mn2+ + ___H+ → ___Pb2+ + ___MnO4- + ___H2O
d) Zn + NO3- + H+→ Zn2+ + NH3OH+ + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Zn + ___NO3- + ___H+→ ___Zn2+ + ___NH3OH+ + ___H2O
e) Cu2O + [Ag(NH3)2]+ + H2O → [Cu(NH3)4]2+ + Cu(OH)2 + Ag
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Cu2O + ___[Ag(NH3)2]+ + ___H2O → ___[Cu(NH3)4]2+ + ___Cu(OH)2 + ___Ag
f) [Cr(OH)6]3- + [Ag(NH3)2]+ + OH- → CrO42- + Ag + NH3 + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___[Cr(OH)6]3- + ___[Ag(NH3)2]+ + ___2OH- → ___CrO42- + ___Ag + ___NH3 + ___H2O
Zadanie R2
Kwas cytrynowy (kwas 2-hydroksypropano-1,2,3-trikarboksylowy) poddany działaniu wodnego roztworu KMnO4 ulega reakcji, w której zostaje przekształcony w kwas acetono-1,3-dikarboksylowy. Jednocześnie obserwuje się powstanie brunatnej zawiesiny i uwalnianie bezbarwnego gazu. Ciało stałe usuwa wprowadzając roztwór szczawianu amonu oraz rozcieńczony roztwór H2SO4 w wodzie. Na końcu, do bezbarwnego roztworu wprowadza się wodę bromową – powoduje to strącenie praktycznie nierozpuszczalnego w wodzie pentabromoacetonu i wydzielenie bezbarwnego gazu.Napisz w formie jonowej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy), równanie reakcji redukcji i równanie reakcji utleniania, które zaszły podczas opisanej przemiany. Uwzględnij środowisko reakcji. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
a) Po dodaniu roztworu KMnO4 do roztworu kwasu cytrynowego.
Równanie redukcji: …………………………………………………………………………………
Równanie utleniania: .......................................................................................................
b) Po wprowadzeniu roztworu szczawianu amonu i roztworu H2SO4.
Równanie redukcji: ………………………………………………………………………………………..
Równanie utleniania:
c) Po wprowadzeniu wody bromowej.Równanie redukcji: ………………………………………………………………………………………..
Równanie utleniania:
Zadanie 2
Mieszaniu cieczy towarzyszy zjawisko kontrakcji objętości, czyli zmiana objętości układu. np. w temperaturze pokojowej po wprowadzeniu do jednego naczynia 100 cm3 etanolu i 100 cm3 czystej wody otrzymuje się ok. 194 cm3 roztworu, zamiast spodziewanych 200 cm3.
Wyjaśnij, dlaczego zjawiska zmniejszenia objętości układu nie obserwuje się po umieszczeniu w jednym naczyniu 100 cm3 n-heksanu i 100 cm3 czystej wody.
Zadanie 3
Temperatura krzepnięcia roztworów jest niższa niż temperatura krzepnięcia czystego rozpuszczalnika. Im więcej drobin wprowadzi się do danej masy rozpuszczalnika, tym niższą temperaturę krzepnięcia ma otrzymany roztwór. Zjawisko obniżenia temperatury krzepnięcia w odniesieniu do temperatury krzepnięcia czystego rozpuszczalnika nazywamy efektem krioskopowym.W dwóch zlewkach (oznaczonych jako I i II)znajdowało się po 500 g wody. Następnie do każdej wprowadzono odpowiednią ilość substancji:
Zlewka I – 0,5 mol glukozy
Zlewka II – 0,5 mol sacharozy
Zlewka III – 0,5 mol chlorku sodu
Zlewka IV – 0,5 mol siarczanu(VI) baru
Zawartość każdej zlewki zamieszano. W każdej stwierdzono obecność fazy ciekłej.Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli informacja jest fałszywa.
Roztwór w zlewce II ma niższą temperaturę krzepnięcia niż roztwór w zlewce I, ponieważ sacharoza jest dwucukrem budowanym z glukozy i fruktozy. P F Ciecz w zlewce III ma taką samą temperaturę krzepnięcia, jak ciecz w zlewce IV P F W jednym naczyniu w praktyce nie zaobserwowano efektu krioskopowego P F Tlenek wapnia w sposób egzotermiczny reaguje z wodą wg równania:
CaO + H2O → Ca(OH)2
Przeprowadzono dwa doświadczenia, przedstawione na schemacie. Wszystkie składniki oraz otoczenie miały początkową temperaturę 25 °C. Temperatura otoczenia nie zmieniła się podczas doświadczenia.
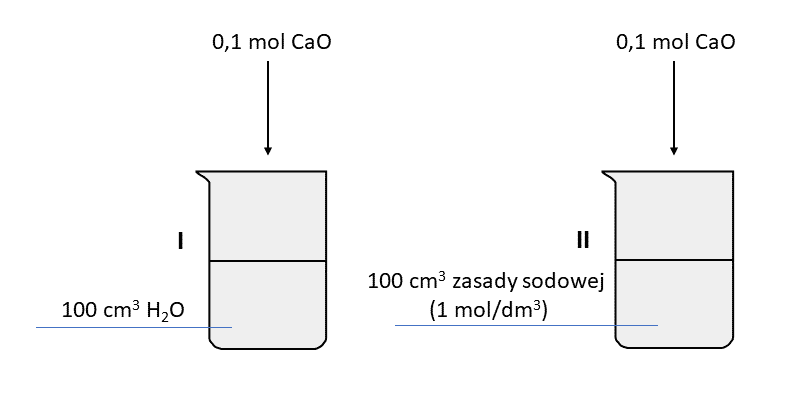
Zadanie 1
Uzupełnij zdania. Wybierz i podkreśl po jednym określeniu z nawiasu.
Po zamieszaniu zawartości temperatura układu w zlewce I była (wyższa od 25 °C / niższa od 25 °C), co oznacza, że układ (zaczął oddawać ciepło do otoczenia / przyjmować ciepło od otoczenia). Po zakończeniu zmian w zlewce I otrzymano (układ jednorodny / zawiesinę).Zadanie 2
W zlewce II zaobserwowano powstanie zawiesiny.
Wybierz zdanie, które w prawidłowo opisuje wynik doświadczenia w zlewce II.
A. W zlewce II nie doszło do zmiany temperatury, ponieważ tlenek wapnia nie reaguje z zasadą sodową.
B. Otrzymanie zawiesiny świadczy o tym, że tlenek wapnia nie reaguje z zasadą sodową.
C. W zlewce II zaszła reakcja, ale jej substraty i produkty są inne niż w zlewce I, więc efekt cieplny jest inny niż w zlewce I. Powstanie zawiesiny nie świadczy o braku reakcji w zlewce II.
D. Tlenek wapnia przereagował z zasadą sodową, a efekt cieplny jest praktycznie taki sam jak w zlewce I. Powstanie zawiesiny nie świadczy o braku reakcji w zlewce II.