Zadania z działu: Efekty energetyczne
Wykonano doświadczenie chemiczne, w którym do rozcieńczonego kwasu solnego wprowadzono w stechiometrycznej ilości roztwór wodorotlenku potasu. Początkowa temperatura użytych roztworów była identyczna i wynosiła 21 °C, podczas gdy po zmieszaniu była znacznie wyższa od początkowej.
Zadanie 1
Zapisz w formie jonowej skróconej równanie reakcji, która zaszła po zmieszaniu roztworów. Uwzględnij teorię Broensteda-Lowry'ego.Zadania 2
Dokończ zdania. Wybierz i podkreśl po jednym określeniu z każdego nawiasu.Entalpia reakcji zobojętniania jest (dodatnia / ujemna), co oznacza, że układ (oddaje ciepło do otoczenia / pobiera ciepło od otoczenia). Na podstawie przeprowadzonego doświadczenia (można stwierdzić, że reakcja autodysocjacji wody jest egzotermiczna / można stwierdzić, że reakcja autodysocjacji wody jest endotermiczna / nie można stwierdzić efektu cieplnego autodysocjacji wody).
Termograwimetria jest metodą analizy termicznej próbek. Wykorzystuje ona bardzo często reakcje rozkładu termicznego z wydzieleniem gazowych produktów, a podstawą analizy jest zmiana (ubytek lub rzadziej przyrost) masy próbki i temperatura, w której dochodzi do zmiany masy próbki.
Magnezyt (minerał o wzorze MgCO3) ulega termicznemu rozkładowi. Po sproszkowaniu, ogrzewany w atmosferze azotu ze stopniowym podnoszeniem temperatury o 10 K/min zaczyna rozkładać się w temperaturze ok. 500 °C z ubytkiem masy. Ubytek masy kończy się po osiągnięciu temperatury 650 °C i rozkład uznaje się za zakończony. Największą szybkość rozkładu obserwuje się w temperaturze ok. 617 °C. Na poniższym rysunku przedstawiono przybliżoną krzywą termograwimetryczną magnezytu (w przeliczeniu na 1 mol próbki).

Kalcyt (minerał o wzorze CaCO3) także ulega termicznemu rozkładowi. Ogrzewany w identycznych warunkach zaczyna się rozkładać po osiągnięciu temperatury 660 °C. Koniec rozkładu obserwuje się ok. 810 °C, a największą szybkość rozkładu obserwuje się ok. 780 °C. Na poniższym rysunku przedstawiono przybliżoną krzywą termograwimetryczną kalcytu (w przeliczeniu na 1 mol próbki).

Zadanie 4.1
Narysuj przybliżoną krzywą termograwimetryczną ogrzewania równomolowej mieszaniny sproszkowanego MgCO3 ze sproszkowanym CaCO3 w podanych warunkach. Przyjmij, że próbka zawiera 1 mol CaCO3.
Zadanie 4.2
Dolomit to minerał węglanowy, którego wzór to MgCa(CO3)2 (lub w postaci adduktywnej to MgCO3·CaCO3). Jest niemal wyłącznym składnikiem skały o tej samej nazwie. Jako skała dolomit występuje w wielu miejscach na całym świecie, są z niego zbudowane niektóre masywy górskie. Ogrzewanie dolomitu do wysokich temperatur prowadzi do jego rozkładu, który składa się z dwóch etapów. W obu etapach powstaje ten sam gaz, a w każdym etapie powstaje połowa gazu. Poddając dolomit analizie termograwimetrycznej w opisanych uprzednio warunkach obserwuje się początek rozkładu po osiągnięciu ok. 600 °C. Największą szybkość rozkładu w pierwszym etapie obserwuje się w temperaturze ok. 745 °C. Początek rozkładu dolomitu następuje w temperaturze o ok. 100 °C wyższej niż obserwuje się w przypadku magnezytu (MgCO3). Drugi etap rozkładu zachodzi najszybciej ok. 780 °C i kończy się w temperaturze ok. 810 °C.a) Oceń poprawność zdań. Zaznacz P, jeśli informacja jest prawdziwa albo F, jeśli informacja jest nieprawdziwa.
Dolomit jest równomolową mieszaniną węglanu wapnia z węglanem magnezu. P F Dolomit może służyć do podnoszenia pH gleb kwaśnych. P F Pozostałość po prażeniu dolomitu do stałej masy stanowią dwa tlenki, z których tylko jeden reaguje z wodą w temperaturze pokojowej. P F
b) Napisz równania reakcji, które zachodzą podczas ogrzewania dolomitu.
Etap I: ………………
Etap II: ………………
c) Wyjaśnij, skąd przekraczająca 100 °C różnica w pomiędzy początkiem rozkładu magnezytu (MgCO3) a początkiem pierwszego etapu rozkładu dolomitu.
Wyjaśnienie: ………
Zadanie 4.3
Neyreryt jest bardzo rzadkim minerałem o wzorze Na2Ca(CO3)2 (Na2CO3·CaCO3). W warunkach pokojowych jest nietrwały i wrażliwy na wilgoć, więc musi być przechowywany w atmosferze ochronnej w hermetycznych pojemnikach. Neyreryt powstaje m.i. w wyniku ogrzewania sproszkowanej mieszaniny dolomitu z węglanem sodu w temperaturach nie przekraczających 500 °C.
a) Napisz równanie reakcji dolomitu z węglanem sodu, w której powstaje neyreryt.
……………………
b) Napisz w formie jonowej równanie reakcji, która zachodzi po wprowadzeniu stałego neyrerytu do wody.
……………………
c) Wyjaśnij, dlaczego podczas ogrzewania do wysokich temperatur mieszaniny dolomitu z węglanem sodu obserwuje się początek uwalniania gazu po osiągnięciu ok. 500 °C, a przy ogrzewaniu czystego dolomitu dopiero po przekroczeniu temperatury 600 °C.
Wyjaśnienie: ..........
W celu określenia czy rozpuszczanie substancji X w wodzie jest procesem egzo- czy endotermicznym wykonano następujące doświadczenie. Do 100 cm3 wody demineralizowanej o temperaturze 20 °C wprowadzono 25 g substancji X i zamieszano. Otrzymano klarowny roztwór o temperaturze 14 °C. Na tej podstawie stwierdzono, że rozpuszczanie substancji X w wodzie jest procesem endotermicznym.
Wiadomo także, że substancję X przechowywano w zamrażarce (w -18 °C) i przed wykonaniem doświadczenia wyjęto z niej. Substancji X użyto natychmiast po wyjęciu z niskiej temperatury.
Rozstrzygnij, czy wykonane doświadczenie pozwala jednoznacznie ustalić znak entalpii procesu rozpuszczania substancji X w wodzie. Uzasadnij swoją opinię.Rozstrzygnięcie: ………………………………..
Uzasadnienie: ………………………………..
Zadanie 5
Poniżej podano efekty energetyczne dwóch reakcji jonowych w stanie standardowym:NaOH(aq) + HCl(aq) → NaCl(aq) + H2O + 55,8 kJ
Ba(NO3)2(aq) + Na2SO4(aq)→ BaSO4(s) + 2NaNO3(aq) + 26,3 kJ
Przeprowadź obliczenia i na podstawie powyższych danych oszacuj standardową entalpię reakcji o podanym równaniu:
Ba(OH)2(aq) + H2SO4(aq) → BaSO4(s) + 2H2O(c)
Tlenek wapnia w sposób egzotermiczny reaguje z wodą wg równania:
CaO + H2O → Ca(OH)2
Przeprowadzono dwa doświadczenia, przedstawione na schemacie. Wszystkie składniki oraz otoczenie miały początkową temperaturę 25 °C. Temperatura otoczenia nie zmieniła się podczas doświadczenia.
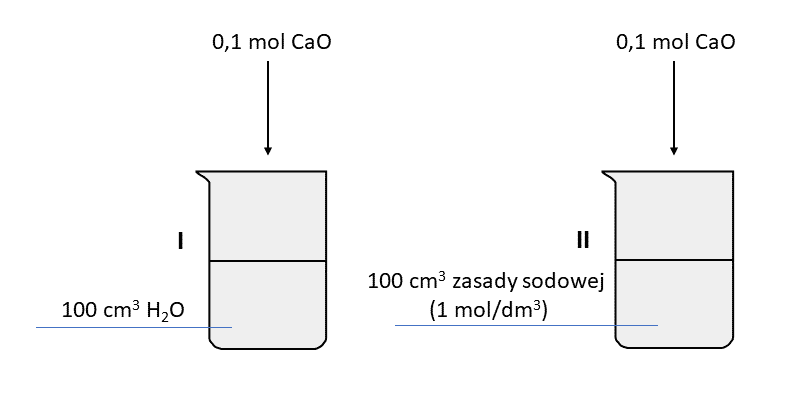
Zadanie 1
Uzupełnij zdania. Wybierz i podkreśl po jednym określeniu z nawiasu.
Po zamieszaniu zawartości temperatura układu w zlewce I była (wyższa od 25 °C / niższa od 25 °C), co oznacza, że układ (zaczął oddawać ciepło do otoczenia / przyjmować ciepło od otoczenia). Po zakończeniu zmian w zlewce I otrzymano (układ jednorodny / zawiesinę).Zadanie 2
W zlewce II zaobserwowano powstanie zawiesiny.
Wybierz zdanie, które w prawidłowo opisuje wynik doświadczenia w zlewce II.
A. W zlewce II nie doszło do zmiany temperatury, ponieważ tlenek wapnia nie reaguje z zasadą sodową.
B. Otrzymanie zawiesiny świadczy o tym, że tlenek wapnia nie reaguje z zasadą sodową.
C. W zlewce II zaszła reakcja, ale jej substraty i produkty są inne niż w zlewce I, więc efekt cieplny jest inny niż w zlewce I. Powstanie zawiesiny nie świadczy o braku reakcji w zlewce II.
D. Tlenek wapnia przereagował z zasadą sodową, a efekt cieplny jest praktycznie taki sam jak w zlewce I. Powstanie zawiesiny nie świadczy o braku reakcji w zlewce II.
W laboratorium, w którym panowała temperatura 21 °C, przygotowano wodny roztwór NH4NO3 w następujący sposób. Stały NH4NO3 i wodę demineralizowaną (oczyszczoną) ogrzano od temperatury otoczenia do 80 °C. Następnie substancje przeniesiono do umieszczonej na stole laboratoryjnym zlewki i zamieszano. Sól uległa całkowitemu rozpuszczeniu. Stwierdzono, że tuż po rozpuszczeniu soli otrzymany roztwór ma temperaturę 65 °C.
Oceń poprawność poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli jest fałszywa.
Rozpuszczanie azotanu(V) amonu w wodzie jest procesem endotermicznym P F W czasie wykonanego doświadczenia układ pobrał ciepło od otoczenia P F Wodorotlenek wapnia jest związkiem trudno rozpuszczalnym w wodzie. W gorącej wodzie jego rozpuszczalność jest nieco niższa niż w zimnej. Związek ten otrzymuje się w egzotermicznej reakcji CaO z wodą. Przeprowadzono doświadczenie, w którym do zlewki z wodą o temperaturze 20 °C wprowadzono stały CaO.
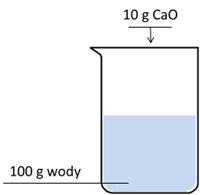
Następnie zamieszano zawartość zlewki.
Zadanie 1.
Nasycony roztwór wodorotlenku wapnia zwiemy wodą wapienną, a wodną zawiesinę tego związku mlekiem wapiennym.
Dokończ zdania. Wybierz i zaznacz jedno określenie spośród podanych w każdym nawiasie.
W opisanym doświadczeniu otrzymano (wodę wapienną / mleko wapienne). Mleko wapienne można otrzymać wprowadzając do wody wapiennej (tlenek wapnia / wodorotlenek wapnia / tlenek lub wodorotlenek wapnia). Wodę wapienną można otrzymać z mleka wapiennego przez wprowadzenie do niego (wody destylowanej / tlenku wapnia ).
Zadanie 2.
Po dodaniu CaO i zamieszaniu zawartości zlewki nie stwierdzono zaniku, ani zmiany barwy ciała stałego.
Wyjaśnij, dlaczego na podstawie powyższej obserwacji nie można zgodzić się ze stwierdzeniem:
Brak widocznych objawów reakcji jest równoznaczny z brakiem reakcji chemicznej.
Odnieś się do stanu układu przed i po zamieszaniu zawartości zlewki.
………………………………………………………………………………………
Zadanie 3.
Z podanych poniżej czynności wybierz te, które należy wykonać, aby potwierdzić, że w opisanym doświadczeniu otrzymano Ca(OH)2. Podkreśl wszystkie prawidłowe czynności.• Wprowadzenie kwasu solnego • Wprowadzenie kropli alkoholowego roztworu fenoloftaleiny • Wprowadzenie zwilżonego uniwersalnego papierka wskaźnikowego u wylotu zlewki • Porównanie temperatury ścianek zlewki przed i po zakończeniu doświadczenia • Dodatek zasady sodowej
Zadanie 4.
Oceń, czy podane poniżej informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.1.
W tej samej temperaturze mleko wapienne ma wyższe pH niż woda wapienna ze względu na wyższy udział Ca(OH)2.
P
F
2.
Ogrzewając wodę wapienną bez dostępu powietrza zaobserwujemy wytrącenie nieznacznej ilości osadu Ca(OH)2.
P
F
3.
Woda wapienna służy do wykrywania CO2 w powietrzu lub innych gazach. Zamiast niej można użyć mleka wapiennego.
P
F