Zadania z działu: Elektrochemia
Twój Redoksownik - pobierz wszystkie zadania z reakcjami redoks w jednym pliku do druku.
Zadanie R29
Aby otrzymać jodan(V) potasu do roztworu chloranu(V) potasu wprowadzono jod. Po dodaniu niewielkiej ilości HNO3 nastąpiła egzotermiczna reakcja, która miała dość szybki przebieg:
2KClO3 + I2 ⟶ 2KIO3 + Cl2Oceń prawdziwość poniższego zdania. Uzasadnij swoją decyzję.
„Z doświadczenia wynika, że jod jest aktywniejszym fluorowcem niż chlor.”
Rozstrzygnięcie: zdanie jest ( prawdziwe / nieprawdziwe ).
Uzasadnienie:
………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Twój Redoksownik - pobierz wszystkie zadania z reakcjami redoks w jednym pliku do druku.
Informacja do zadań R26 – R28
ClO2 jest trującym tlenkiem chloru, który w temperaturze pokojowej jest pomarańczowoczerwonym gazem, pod ciśnieniem 1013 hPa skrapla się po ochłodzeniu do temperatury niższe od 11 °C. Jedna z laboratoryjnych metod jego otrzymywania polega na działaniu stężonego roztworu H2SO4 na KClO3. Schemat tej reakcji przedstawiono poniżej (metoda I):
KClO3 + H2SO4 ⟶ HClO4 + ClO2 + KHSO4 + H2O
Inna metoda polega na działaniu roztworem H2SO4 na stechiometryczną mieszaninę KClO3 z kwasem szczawiowym (H2C2O4) (metoda II).
KClO3 + H2C2O4 + H2SO4 ⟶ ClO2 + CO2 + KHSO4 + H2O
Zadanie R26
Zapisz w formie jonowej skróconej równanie redukcji i równanie reakcji utleniania zachodzących podczas otrzymywania ClO2 w wyniku działania stężonego roztworu H2SO4 na KClO3. Podaj stosunek molowy utleniacza i reduktora.
Równanie redukcji: …………………………………………………………………………………………………….
Równanie utlenienia: ………………………………….……………………………………………………………….
nutl. : nred. = …………………….Zadanie R27
Zapisz w formie jonowej skróconej równanie reakcji utleniania zachodzącej podczas otrzymywania ClO2 w wyniku działania stężonego roztworu H2SO4 na mieszaninę KClO3. Z kwasem szczawiowym. Uzupełnij współczynniki stechiometryczne, aby otrzymać sumaryczne równanie reakcji utleniania i redukcji.Równanie utlenienia: ………………………………….……………………………………………………………….
….KClO3 + ….H2C2O4 + ….H2SO4 ⟶ ….ClO2 + ….CO2 + ….KHSO4 + ….H2O
Zadanie R28
Rozstrzygnij, która z przedstawionych metod (I czy II) jest lepszym źródłem ClO2 ze względu na zużycie KClO3.
Rozstrzygnięcie: ………………………………………………………….
Uzasadnienie:...................................................
Twój Redoksownik - pobierz wszystkie zadania z reakcjami redoks w jednym pliku do druku.
Zadanie R25
W wyniku redukcji manganianów(VII) można otrzymać manganiany(VI). Roztwory manganianów(VI) litowców mają charakterystyczna ciemnozieloną barwę. Jony manganianowe(VI) mają niezbyt silne właściwości utleniające. Poniżej przedstawiono wartości standardowych potencjałów redukcji dla odpowiednich półogniw.
Reakcja połówkowa E°, V MnO4– + e ⟶ MnO42– +0,558 MnO42– + 2H2O + 2e ⟶ MnO2 + 4OH– +0,60 Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa albo F, jeśli informacja jest fałszywa.
1. Jony manganianowe(VI) maja zdolność do dysproporcjonowania w roztworach wodnych. P F 2. Podniesienie pH zwiększa trwałość jonów manganianowych(VI). P F Twój Redoksownik - pobierz wszystkie zadania z reakcjami redoks w jednym pliku do druku.
Zadanie R24
Tal tworzy dwa kationy proste, które mogą występować w roztworach wodnych. Poniżej podano standardowe potencjały redukcji dla półogniw, w których zachodzą następujące reakcje połówkowe:Reakcja połówkowa E°, V Tl+ + e ⟶ Tl –0,336 Tl3+ + 2e ⟶ Tl+ +1,252 Z fluorem tworzy trwałe związki o wzorach TlF oraz TlF3, w których kationy talu różnią się ładunkiem. Związek o wzorze TlI3 można otrzymać w reakcji wg równania:
TlI + I2 ⟶ TlI3
a) Zapisz w formie jonowej skróconej równanie reakcji talu z kwasem rozcieńczonym kwasem solnym użytym w nadmiarze. Uwzględnij, że powstająca sól nieznacznie rozpuszcza się w wodzie o temperaturze pokojowej.………………………………………………………………………………………………………………………….
b) Ustal, czy związek o wzorze TlI3 to związek talu(I) czy talu(III). Uzupełnij schemat, wpisz wzór sumaryczny kationów i anionów obecnych w kryształach TlI3.
Stopień utlenienia talu: ………………….wzór kationu wzór anionu
Pobierz wszystkie zadania ze schematów ogniw w pliku do druku w formacie pdf (kliknij).
Artykuł wyjaśniający zasady konwencji sztokholmskiej (kliknij).
Zadanie 1
Na podstawie schematycznego rysunku ogniw galwanicznych zapisz schemat danego ogniwa w konwencji sztokholmskiej.A)

schemat: (-) ………………………………………………………………………………………………………..(+)
B)

schemat: (-) ………………………………………………………………………………………………………..(+)
C)

schemat: (-) ………………………………………………………………………………………………………..(+)
D)

schemat: (-) ………………………………………………………………………………………………………..(+)
E)

schemat: (-) ………………………………………………………………………………………………………..(+)
F)

schemat: (-) ………………………………………………………………………………………………………..(+)
G)

schemat: (-) ………………………………………………………………………………………………………..(+)
H)

schemat: (-) ………………………………………………………………………………………………………..(+)
I)

schemat: (-) ………………………………………………………………………………………………………..(+)
J)
schemat: (-) ………………………………………………………………………………………………………..(+)
K)

schemat: (-) ………………………………………………………………………………………………………..(+)
L)

schemat: (-) ………………………………………………………………………………………………………..(+)
M)

schemat: (-) ………………………………………………………………………………………………………..(+)
N)

schemat: (-) ………………………………………………………………………………………………………..(+)
O)

schemat: (-) ………………………………………………………………………………………………………..(+)
Zadanie 2
Poniżej podano standardowe potencjały redukcji wybranych reakcji połówkowych zachodzących w standardowych półogniwach. Półogniwa te oznaczono symbolami od A do F.
Przez połączenie odpowiednich półogniw zmontowano standardowe ogniwa galwaniczne.
Zadanie 2.1
Napisz w formie jonowej skróconej sumaryczne równanie reakcji redoks zachodzącej w pracującym ogniwie oraz zapisz schemat tego ogniwa zgodnie z konwencją sztokholmską. W odpowiednich przypadkach przyjmij, że elektrodą jest platyna.
A z C)
Równanie reakcji:
……………………………………………………………………………………………………………………………….
schemat: (-) ……………………………………………………………………………….………………………...Pt(+)C z D)
Równanie reakcji:
……………………………………………………………………………………………………………………………….
schemat: (-)……..……………………………………………………………………………………………………...(+)D z E)
Równanie reakcji:
……………………………………………………………………………………………………………………………….
schemat: (-) ………………………………………………………………………………………………….....…..(+)E z F)
Równanie reakcji:
……………………………………………………………………………………………………………………………….
schemat: (-) ………………………………………………………………………………………………….....…..(+)
Zadanie 2.2
Podaj wzór substancji lub jonu, który w podanym zestawie pełni następującą funkcję.
Najsłabszy utleniacz: ……………
Najsłabszy reduktor: …………….Zadanie 3
Na podstawie schematu ogniwa galwanicznego uzupełnij graficzne przedstawienie ogniwa. Wpisz brakujące symbole lub wzory w puste miejsca. Napisz w formie jonowej skróconej sumaryczne równanie reakcji redoks zachodzącej w pracującym ogniwie.
A) schemat: (-)Pt | CrO42–, Cr(OH)6]3–, OH– || Br–, BrO3–, OH– | Pt(+)

Równanie reakcji: ………………………………………………………………………………………………………..
B) schemat: (-)Pt | Sn2+, Sn4+ || Pb2+, H3O+ | PbO2 | Pb(+)

Równanie reakcji: ………………………………………………………………………………………………………..
Zadanie R5
Po zmieszaniu wodnego roztworu azotanu(V) srebra(I) z wodnym roztworem nadtlenodisiarczanu potasu dochodzi do wytrącenia brunatnoczarnego osadu. Schemat reakcji przedstawiono poniżej.
AgNO3 + K2S2O8 + H2O → Ag4O4 + KHSO4 + HNO3
Zadanie R5.1
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie.
Równanie redukcji:………………..
Równanie utleniania:……………..
Zadanie R5.2
Związek o wzorze Ag4O4 ma bardzo silne właściwości utleniające. Potraktowany stężonym kwasem azotowym roztwarza się tworząc roztwór o intensywnej barwie brunatnej. W roztworze tym srebro istnieje w postaci dwudodatnich kationów. Po rozcieńczeniu tego roztworu w wodzie ponownie strąca się Ag4O4.
Napisz w postaci cząsteczkowej równanie reakcji zachodzącej po wprowadzeniu stałego Ag4O4 do stężonego kwasu azotowego(V) (równanie I) oraz po rozcieńczeniu otrzymanego roztworu w wodzie (równanie II).Równanie I: ………………..
Równanie II: …………….....
Zadanie R5.3
Na podstawie przedstawionych informacji określ trwałość kationów srebra w wodnym środowisku w zależności od stopnia utlenienia. Dokończ zdania. Wybierz i podkreśl jedną z odpowiedzi z podanych w nawiasach.
Kationy Ag+ są (trwałe / nietrwałe) w wodnym środowisku.
Kationy Ag2+ są (trwałe / nietrwałe) w wodnym środowisku.
Zadanie R4
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie. Napisz w formie jonowej skróconej sumaryczne równanie reakcji utleniania i redukcji.
a) S2O32- + I2 → S4O62- + I-
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___S2O32- + ___I2 → ___S4O62- + ___I-
b) Ag4O4 + Sn2+ + H+ → Ag + Sn4+ + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Ag4O4 + ___Sn2+ + ___H+ → ___Ag + ___Sn4+ + ___H2O
c) PbO2 + Mn2+ + H+ → Pb2+ + MnO4- + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___PbO2 + ___Mn2+ + ___H+ → ___Pb2+ + ___MnO4- + ___H2O
d) Zn + NO3- + H+→ Zn2+ + NH3OH+ + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Zn + ___NO3- + ___H+→ ___Zn2+ + ___NH3OH+ + ___H2O
e) Cu2O + [Ag(NH3)2]+ + H2O → [Cu(NH3)4]2+ + Cu(OH)2 + Ag
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Cu2O + ___[Ag(NH3)2]+ + ___H2O → ___[Cu(NH3)4]2+ + ___Cu(OH)2 + ___Ag
f) [Cr(OH)6]3- + [Ag(NH3)2]+ + OH- → CrO42- + Ag + NH3 + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___[Cr(OH)6]3- + ___[Ag(NH3)2]+ + ___2OH- → ___CrO42- + ___Ag + ___NH3 + ___H2O
Przeprowadzono doświadczenie zilustrowane poniższym schematem.
Celem doświadczenia było odróżnienie dwóch, oznaczonych umownie literami X i Z, metali, z których wykonano płytki. Wiadomo, że jednym metalem był cynk, a drugim – nikiel.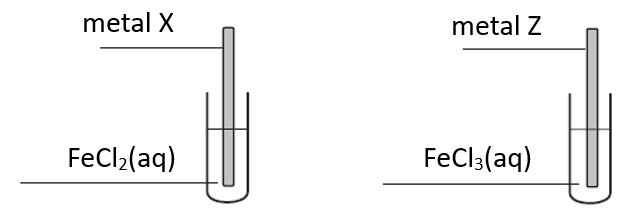
Po pewnym czasie płytki wyjęto z roztworów i osuszono. Zważono płytkę wykonaną z metalu X i stwierdzono, że masa tej płytki uległa zmianie.
Zadanie 1
Uzupełnij poniższe zdania. Wybierz i zaznacz właściwe określenie spośród podanych w każdym nawiasie oraz napisz w formie jonowej skróconej równanie zachodzącej reakcji.
Masa płytki wykonanej z metalu X się (zmniejszyła / zwiększyła), a podczas przeprowadzonego doświadczenia przebiegła reakcja zilustrowana równaniem:
.................................................................................................
Metalem Z był (cynk / nikiel).
Zadanie 2
Rozstrzygnij, czy do odróżnienia metali od siebie wystarczająca jest informacja, że masa płytki wykonanej z metalu X uległa zmianie. Wybierz po jednym określeniu z każdego nawiasu.
Odróżnienie metali na podstawie tej informacji (jest / nie jest) możliwe, ponieważ w czasie trwania doświadczenia masa płytki wykonanej z metalu Z się (także się zmniejszyła / także się zwiększyła / nie uległa zmianie). W naczyniu, w którym umieszczona była płytka z metalu Z (sól żelaza pozostała niezmieniona / powstała inna sól żelaza / powstało metaliczne żelazo).