Zadania z działu: Chemia organiczna
Ugrupowanie nadtlenkowe występuje w cząsteczkach kwasu Caro H2SO5 oraz kwasu nadtlenooctowego CH3COOOH. Jeden z atomów tlenu, którym przypisuje się -I formalny stopień utlenienia wiąże się z atomem wodoru. Podstawienie jednej z grup –OH w cząsteczce kwasu siarkowego(VI) atomem chloru prowadzi do kwasu chlorosulfonowego HSO3Cl. Kwas Caro można otrzymać w reakcji kwasu chlorosulfonowego z nadtlenkiem wodoru, jak przedstawia równanie:
HSO3Cl + H2O2 → H2SO5 + HCl
Napisz równanie reakcji otrzymywania kwasu nadtlenooctowego opisaną metodą.…………………………
Zadanie R11
Reakcja fenoli o skondensowanych pierścieniach aromatycznych w swoich cząsteczkach przebiega inaczej niż w przypadku fenoli o jednym pierścieniu aromatycznym w swoich cząsteczkach. Schemat reakcji przedstawiono poniżej.
Napisz w formie jonowej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji redukcji i równanie reakcji utleniania, które zaszły podczas opisanej przemiany. Zastosuj wzory półstrukturalne (grupowe) związków organicznych. Podaj molowy stosunek utleniacza do reduktora.
Równanie redukcji: ………………………………………………………………………………………..
Równanie utleniania:
nutl. : nred. = ……………………..
Ozonoliza polega na rozrywaniu wiązań wielokrotnych pomiędzy atomami węgla. W pierwszym etapie związek organiczny poddaje się działaniu ozonu (O3), w wyniku czego powstaje ozonek organiczny. Na poniższym schemacie przedstawiono równanie addycji ozonu do alkenu o nierozgałęzionym łańcuchu węglowym.

Ozonki tego typu nie są zbyt trwałe, tj. są podatne zarówno utlenianie, jak i redukcję. Kolejne etapy mogą więc polegać zarówno na częściowej redukcji (ozonoliza redukcyjna) lub dalszemu utlenianiu ozonku organicznego (ozonoliza oksydacyjna).

W wyniku rozerwania wiązania C=C na końcu łańcucha węglowego powstaje tylko jeden kwas organiczny, zaś uboczne produkty stanowią CO2 i woda. Ozonoliza znalazła zastosowanie przy produkcji niektórych kwasów karboksylowych.
Zadanie 1
Z podanych odczynników wybierz ten, którego należy użyć w odpowiednim wariancie ozonolizy.
H2O2(aq); Zn
Wariant I: …………………
Wariant II: ………………..Zadanie 2
Poniżej przedstawiono schemat termicznego rozkładu kwasu rycynolowego.

Produkty rozkładu rozdziela się, a jeden z nich (kwas undecylenowy) poddaje się oksydacyjnej ozonolizie, której organicznym produktem jest kwas sebacynowy.
a) Podaj nazwę systematyczną kwasu sebacynowego.
………………………………………………………………………………….
b) W wyniku ozonolizy redukcyjnej pewnego alkenu otrzymuje się jako jedyny produkt organiczny ten sam aldehyd, który powstaje w wyniku termicznego rozkładu kwasu rycynolowego.
Narysuj uproszczony wzór kreskowy tego alkenu…………………………………………………………………………………………………
Zadanie 3
Acyloiny to związki organiczne będące 𝛂-hydroksyketonami. Jedna z metod ich otrzymywania to tzw. kondensacja acyloinowa, polegajaca na reakcji estru z metalicznym sodem, a następnie na hydrolizie powstałej soli sodowej benzoiny. Jeśli reakcji poddano estry metylowe, to poza acyloiną ostatecznymi produktami są także metanol i wodorotlenek sodu. Schemat tej reakcji przedstawiono na poniższych schemacie.
Jeśli reakcji z sodem poddać związek, w którego cząsteczce znajdują się dwa ugrupowania estrowe, to reakcja kondensacji acyloinowej może zajść pomiędzy grupami estrowymi w obrębie jednej cząsteczki.
a) Napisz, ile moli sodu potrzeba, aby poprzez redukcję etanianu etylu powstał 1 mol odpowiedniej acyloiny.
………………………………………………………………………………
b) kwas sebacynowy poddano estryfikacji nadmiarem metanolu, a otrzymany ester poddano reakcji z sodem, a otrzymany produkt poddano hydrolizie.
Narysuj wzór uproszczony (kreskowy) lub półstrukturalny acyloiny, która powstaje w wyniku wewnątrzcząsteczkowej kondensacji estru kwasu sebacynowego.
Zadanie R9
W wyniku katalizowanej przez oksydazę glukozową reakcji powstaje glukonolakton (C6H10O6). Schemat reakcji przedstawiono poniżej.

W kolejnym etapie nadtlenek wodoru jest rozkładany na wodę i tlen.
Zadanie R9.1
a) Napisz w formie jonowej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji redukcji i równanie reakcji utleniania, które zaszły podczas opisanej przemiany. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.Równanie redukcji: ………………………………………………………………………………………..
Równanie utleniania:
b) Uzupełnij schemat reakcji tak, aby otrzymać sumaryczne równanie dwuetapowego procesu, w którym powstaje glukonolakton.
……C6H12O6 + …….O2 → ……C6H10O6 + …….H2OZadanie R9.2
Atom węgla związany bezpośrednio z atomem, którego orbitalom walencyjnym przypisujemy hybrydyzację sp2, nazywamy atomem 𝛂, kolejny atomem β, a następne γ, δ, ε itd.
Uzupełnij zdania. Wpisz symbol atomu węgla i wybierz po jednym określeniu z nawiasu.
W wyniku reakcji glukoza zostaje przekształcona w glukono-…..-lakton. Otrzymanie tego związku możliwe jest (wyłącznie z formy 𝛂 / wyłącznie z formy β / z dowolnego anomeru) glukozy. Glukono-…..-lakton należy do (ketonów / kwasów karboksylowych / estrów).
Zadanie R7
Anilina to najważniejsza amina aromatyczna. Główną metodą produkcji aniliny jest to redukcja nitrobenzenu. Najstarszą przemysłową metodą produkcji aniliny jest tak zwany proces Bechampa. Poniżej przedstawiono schemat reakcji zachodzącej podczas tego procesu:
C6H5NO2 + Fe + H2O → C6H5NH2 + Fe3O4
a) Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji redukcji oraz równanie reakcji utleniania zachodzących podczas opisanej przemiany. Uwzględnij, że proces biegnie w obecności katalitycznych ilości kwasu solnego.równanie redukcji: .................................................................
równanie utleniania: ..............................................................
b) Uzupełnij współczynniki stechiometryczne w poniższym schemacie.
....C6H5NO2 + ....Fe + ....H2O → ....C6H5NH2 + ....Fe3O4
W celu otrzymania propanalu zaplanowano przeprowadzić reakcję, którą opisuje równanie stechiometryczne:
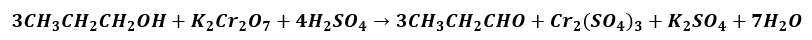
W metodzie tej stosuje się wodny zakwaszony roztwór K2Cr2O7. Ze względu na podatność aldehydu na dalsze utlenianie do kwasu karboksylowego stosuje się nadmiar alkoholu. Z mieszaniny poreakcyjnej łatwo wydzielić aldehyd metodą destylacji, więc reakcję przeprowadza się w odpowiedniej aparaturze. Jeden z odczynników podawany jest z wkraplacza po kropli do kolby reakcyjnej, w której znajduje się mieszany drugi odczynnik. Napisz, który zestaw jest prawidłowo zaplanowany, by wydajność otrzymywania aldehydu była jak najwyższa? Uzasadnij swój wybór.
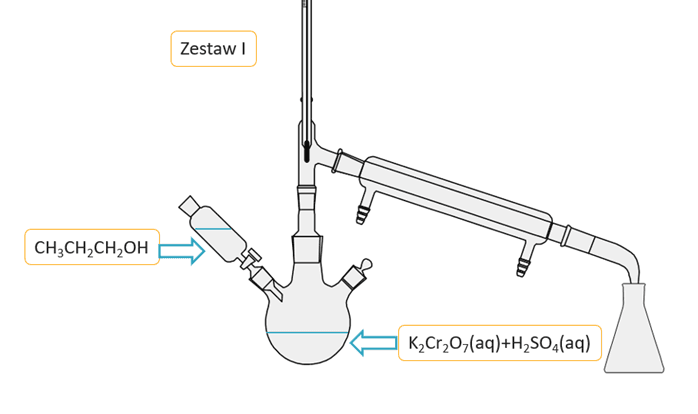
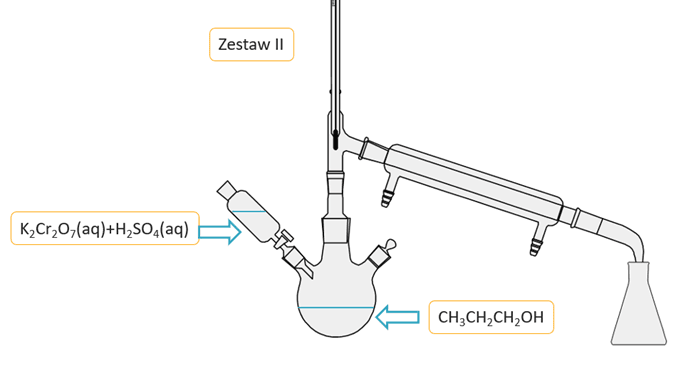
Zestaw:........
Uzasadnienie:...........
Prezentowane zadanie jest autorską propozycją jak mogłoby wyglądać zadanie nr 17 z arkusza maturalnego z 16.05.2024. Propozycja ta wynika z dyskusyjnego zachowania styrenu (w oryginalnym zadaniu 17) w prezentowanych warunkach. W tej propozycji styren zastąpiono cykloheksyloetenem.
Zadanie 17
Cykloalkany ulegają analogicznym reakcjom jak alkany.
Benzen, cykloheksan i winylocykloheksan to węglowodory, które w temperaturze pokojowej są bezbarwnymi cieczami. Ich wzory przedstawiono poniżej:
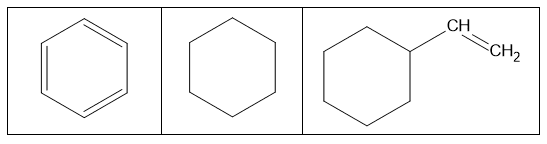
W trzech naczyniach znajdowały się oddzielnie i w przypadkowej kolejności: benzen, cykloheksan i winylocykloheksan. W celu identyfikacji tych substancji wykonano dwuetapowe doświadczenie. W pierwszym etapie do trzech probówek zawierających wodny roztwór manganianu(VII) potasu w środowisku obojętnym wprowadzono po jednej z badanych substancji. Następnie każdą probówkę zamknięto korkiem i wstrząśnięto. Po pewnym czasie zawartości probówek przybrały wygląd pokazany na zdjęciach.

W pierwszym etapie zidentyfikowano jeden z trzech węglowodorów. W drugim etapie doświadczenia do próbek niezidentyfikowanych węglowodorów wprowadzono stężony kwas azotowy(V) z dodatkiem stężonego kwasu siarkowego(VI) – i ogrzano zawartości probówek. Wyniki drugiego etapu doświadczenia przedstawiono na poniższych zdjęciach.
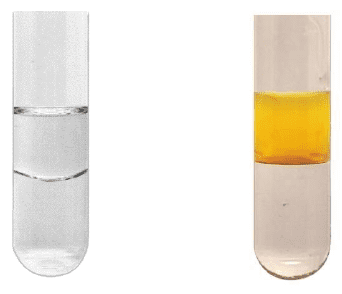
Zadanie 17.1
Napisz wzór sumaryczny związku manganu, który powstał w wyniku reakcji zachodzącej w pierwszym etapie doświadczenia, oraz wzór półstrukturalny (grupowy) lub uproszczony organicznego produktu tej przemiany.
Zadanie 17.2
Napisz równanie reakcji, która umożliwiła odróżnienie związków w drugim etapie doświadczenia.
..........................................
Zadanie to jest autorską propozycją jak mogłoby wyglądać zadanie nr 27 z arkusza maturalnego z 16.05.2024 (F2023), aby było ono jednoznaczne
i zgodnie z właściwościami chemicznymi przedstawionych substancji.Przeprowadzono reakcje zgodnie ze schematem:
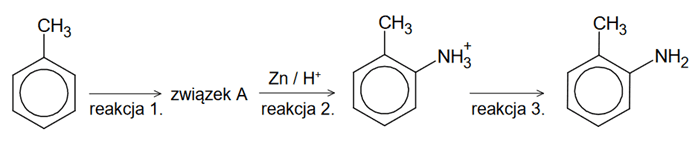
Do organicznego związku w reakcji 1. wkraplano brom w obecności światła. Wkraplanie przerwano, gdy osiągnięto stosunek molowy substancji 1 : 1.
Zadanie 27
Narysuj wzór półstrukturalny lub uproszczony organicznego produktu opisanej reakcji i uzupełnij zdanie. Wybierz i zaznacz właściwą odpowiedź spośród podanych w nawiasie.
Opisana przemiana (jest / nie jest) reakcją utlenienia-redukcji.
Komentarz autora: informacja do zadania w oryginalnym brzmieniu mówi o produkcie reakcji 3 (2-metyloaniliny) i jego dalszej reakcji z bromem. Niestety, ale obecność grupy -NH2 związanej z pierścieniem aromatycznym silnie aktywuje pierścień w reakcjach substytucji elektrofilowe (anilina w reakcji z wodą bromową daje prawie natychmiast osad 2,4,6-tribromoaniliny - bez żadnych katalizatorów). Z tego też powodu zmieszanie z bromem może doprowadzić do bardzo gwałtownej reakcji (a nawet wybuchu) po zmieszaniu reagentów i bez udziału światła. Finalnym produktem powinna być 2,4-dibromo-6-metyloanilina, a w przypadku stosunku molowego 1 : 1 mieszanina 2,4-dibromo-6-metyloaniliny, 2-bromo-6-metyloaniliny i 4-bromo-6-metyloaniliny. Grupa -NO2 jest podstawnikiem bardzo silnie dezaktywujacym pierścień aromatyczny - po zmieszaniu w bromem reakcja powinna zajść dopiero przy naświetlaniu, analogicznie jak w przypadku bromowania toluenu na świetle. Związek taki pojawia się jako związek A (produkt reakcji 1).
Zadanie z kwasem mrówkowym i próbą Trommera, jakie mogłoby pojawić się na maturze 😊
Przypominam też, że NIE MUSICIE WIEDZIEĆ, CZY KWAS MRÓWKOWY ULEGA PRÓBIE TROMMERA ALBO TOLLENSA. MACIE TYLKO WIEDZIEĆ, ŻE KWAS TEN MA (WOBEC SILNYCH UTLENIACZY) WŁAŚCIWOŚCI REDUKUJĄCE. Dalsze informacje dla tegorocznych maturzystów znajdują się pod treścią zadania.
Przeprowadzono serię doświadczeń, w których porównywano zachowanie dwóch reduktorów organicznych: metanalu i kwasu metanowego (mrówkowego) wobec różnych utleniaczy w wodnym środowisku: roztwór wodorotlenku diaminasrebra i zalkalizowana zawiesina wodorotlenku miedzi(II). W doświadczeniach nr 4 i 5 użyto takiej ilości zasady, by dodany kwas metanowy nie spowodował zmiany odczynu mieszaniny reakcyjnej na obojętny lub kwasowy. Wyniki doświadczenia przedstawiono w tabeli. Pewne miejsce pozostawiono jednak puste, a w pozostałych przypadkach podano niektóre z objawów reakcji.
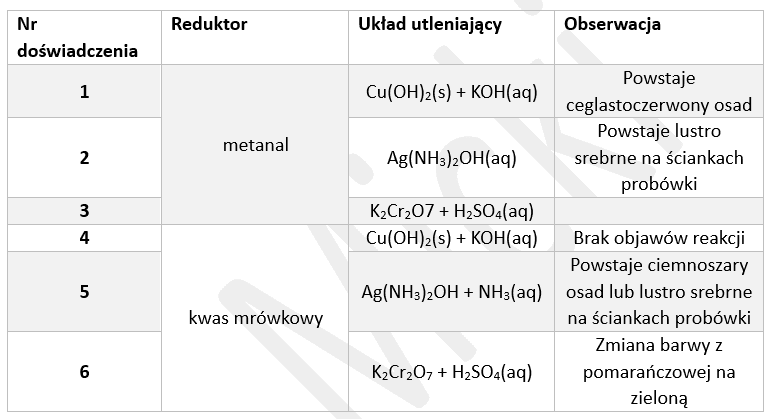
Uzupełnij poniższe zdania. Wybierz i podkreśl jedno wyrażenie z podanych w nawiasach.
Można stwierdzić, że metanal ma (silniejsze / słabsze) właściwości redukcyjne, niż kwas metanowy. W zasadowym środowisku, spośród Cu(OH)2(s) i [Ag(NH3)2]+ silniejszym utleniaczem jest ten (pierwszy / drugi). Na podstawie wyniku doświadczenia nr 6 można stwierdzić, że roztwór reakcyjny w doświadczeniu nr 3 (pozostał pomarańczowy / zmienił barwę z pomarańczowej na żółtą / zmienił barwę z pomarańczowej na zieloną). Uwalnianie się bezbarwnego gazu zaobserwowano w doświadczeniu nr 6. Gaz ten (powstawał także / nie powstawał) w doświadczeniu nr 5.
********************************************
W 2015 roku pojawiło się zadanie dotyczące zachowania kwasu mrówkowego w próbie Trommera. Z INFORMACJĄ WSTĘPNĄ, bo jak piszę - nigdy nie było w wymaganiach, by znać zachowanie tego kwasu w próbie Trommera czy Tollensa. Takie zadanie już więcej się nie pojawiło, ponieważ:
w CKE juz od dawna wiedzą, że kwas ten nie ulega próbie Trommera,
dawniej maturę przygotowywano na podstawie informacji z podręczników szkolnych (którymi zresztą żyje większość chemików). Obecnie treści te są bardziej weryfikowane i jest coraz mniej bubli na maturze, a pewnych rzeczy NIE MA JUŻ WCALE NA maturze z chemii. Bo wiadomo, że były błędne, że pewne rzeczy w podręcznikach są błędne. I nie jest ich mało,
informacja do zadania z 2015 była błędna: oparta na podręcznikowych przekłamaniach, ponadto opis był niezgodny z procedurą przeprowadzania próby Trommera - taki jak do dziś serwują podręczniki szkolne,
Jeśli sami porównacie nowsze i starsze arkusze, to sami zauważycie sporą różnicę w opisach próby Trommera i Tollensa w treści zadań.
No dobra, ale to, że zadanie z 2015 roku było bublem i więcej takowego nie będzie. Ale to nie oznacza, że o ten kwas w ogóle nie będą pytać. Że nie będzie jakiegoś redoksa albo czegoś innego z tym kwasem. Rok temu wymyśliłem takie zadanie, które ma pokazać, jakich zadań co do HCOOH możnaby się spodziewać po skorygowaniu wiadomości co do zachowania się HCOOH.
To, że się dowiedzieli o tym, że HCOOH nie ulega próbie Trommera nie spowodowało, że system egzaminowania padł, a w CKE wszyscy poszli z torbami. Nie po raz pierwszy informacja dotycząca czegoś nie pokrywa się z jakimś starszym arkuszem. Dlatego uważam, że ze zbiorów zadań bazujących na kopiuj+wklej z arkuszy CKE należy pewne zadania powywalać, bo dziś wprowadzają w błąd i są źródłem zamieszania. Tak więc to, że raz palnęli: "HCOOH ulega próbie Trommera" nie oznacza, że "na maturze piszemy, że HCOOH ulega próbie Trommera". A co zrobicie, jak serio dostaniecie takie zadanie podobne do tego? Odpowiecie sprzecznie z podaną infomacją do zadania, bo na maturze piszemy że... Czy raczej wywnioskujecie coś z tej informacji?
A jeśli ktoś będzie miał zagwozdkę "dlaczego takie odpowiedzi?" to niech sobie spróbuje zapisać równanie albo chociaż schemat reakcji - z uwzględnieniem środowiska, w którym ta reakcja zachodzi ☺
W wyniku całkowitego spalenia pary węglowodoru X otrzymano 7,5 dm3 (w przeliczeniu na warunki normalne) spalin zawierających tylko CO2 i H2O. Po wykropleniu pary wodnej pozostały gaz zajmuje w warunkach normalnych objętość 5 dm3. Gęstość par węglowodoru X jest 3 razy większa niż gęstość etynu (mierzona w identycznych warunkach).
Ustal nazwę węglowodoru X.