Zadania z działu: Chemia ogólna
W temperaturze 0 °C rozpuszczalność stałego jodku sodu w ciekłym SO2 wynosi 15 g na 100 g rozpuszczalnika. W tych warunkach w równowadze z roztworem nasyconym są kryształy o wzorze NaI·4SO2.
Przygotowano 200 g roztworu jodku sodu w ciekłym SO2, nasyconego w temperaturze 0 °C. Roztwór przechowywano w szczelnie zamkniętej ampule w temperaturze 0 °C. Po pewnym czasie ostrożnie otwarto ampułę, co poskutkowało odparowaniem części rozpuszczalnika i wydobywaniem się gazowego SO2 na zewnątrz. Ampułę zamknięto po kilku minutach i stwierdzono, że masa jej zawartości spadła o 20 g. Ampułę ponownie umieszczono w temperaturze 0 °C i pojawiły się w niej kryształy.Zadania 1
Oblicz masę wydzielonych kryształów.Zadania 2
Podaj stężenie (w procentach masowych) roztworu nad wydzielonymi kryształami.Zadania 3
Dokończ zdania. Wybierz po jednym określeniu z każdego nawiasu. Uzasadnij wybór.Należy się spodziewać, że w temperaturze 0 °C rozpuszczalność NaI w ciekłym CO2 jest (na zbliżonym poziomie jak w / znacznie niższa niż / znacznie wyższa niż) w ciekłym SO2. Wynika to z faktu, że CO2 jest rozpuszczalnikiem …………………………… a SO2 jest rozpuszczalnikiem …………………………. . Różny charakter CO2 i SO2 jako rozpuszczalników wynika z różnicy w budowie ich cząsteczek. Cząsteczka SO2 ma kształt (liniowy / kątowy / piramidy trygonalnej), a cząsteczka CO2 ma kształt (liniowy / kątowy / piramidy trygonalnej).
Dokończ zdania, wybierając po jednej odpowiedzi z każdego nawiasu.
Cząsteczka SO3 ma strukturę (płaską/przestrzenną), a cząsteczka NH3 (płaską/przestrzenną). Cząsteczka BeBr2 ma kształt (tetraedryczny / piramidy trygonalnej / kątowy/liniowy), a cząsteczka wody ma kształt (tetraedryczny / piramidy trygonalnej / kątowy / liniowy), co wynika z obecności (wiązań typu σ / orbitali niezhybrydyzowanych / wolnych par elektronowych/wiązań koordynacyjnych) w przypadku tej drugiej. Pośród związków: NaCl i CO – (oba związki / tylko NaCl / tylko CO) tworzy cząsteczki liniowe.
Trinitroamid to związek z grupy tlenków azotu o sumarycznym wzorze N4O6. Jednemu z atomów azotu w cząsteczce tego związku przypisuje się zerowy stopień utlenienia, a pozostałym atomom azotu przypisuje się hybrydyzację orbitali walencyjnych typu sp2. Wiadomo, że wszystkie atomy mają konfigurację neonu.
W oparciu o powyższe informacje narysuj wzór elektronowy trwałej struktury cząsteczki trinitroamidu. Zaznacz za pomocą kresek wszystkie wiążące i wolne pary elektronowe.
Zadanie 6
Kwas cytrynowy jest kwasem trójprotonowym. Z przesyconych roztworów kwasu cytrynowego (C6H8O7) w wodzie wypadają kryształy o wzorze C6H8O7·xH2O. W celu ustalenia współczynnika x próbkę kryształów o masie 1,211 g (otrzymanych z wodnego roztworu) rozpuszczono w wodzie i miareczkowano roztworem NaOH w obecności fenoloftaleiny. Do pojawienia się trwałego różowego zabarwienia zużyto 69,2 cm3 roztworu NaOH o stężeniu 0,2500 mol/dm3.
Zadanie 6.1
Oblicz wartość współczynnika x.Zadanie 6.2
Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli informacja jest fałszywa.
W opisanym hydracie kwasu cytrynowego na jedną cząsteczkę kwasu przypada jedna cząsteczkę wody, a w hydracie o wzorze CuSO4·5H2O na jedną cząsteczkę soli przypada pięć cząsteczek wody. P F Rozpuszczenie w wodzie bezwodnego kwasu cytrynowego i pozostawienie do odparowania wody prowadzi do otrzymania kryształów o wzorze C6H8O7·H2O P F Kwas cytrynowy może reagować z NaOH w stosunku molowym nkwasu : nNaOH = 1 : 1. P F Znanych jest wiele syntetycznych radioizotopów niklu. Część z nich o niższych liczbach masowych ulega rzadziej obserwowanym typom rozpadów. Jądra atomowe niklu-48 rozpadają się wg różnych ścieżek, które zachodzą w tym samym czasie.
Zadanie 1
Jednym z produktów jest żelazo-46 oraz cząstki oznaczone umownie symbolem X.
Ustal symbol cząstki X i napisz równanie opisanej przemiany. Uzupełnij wszystkie pola w poniższym schemacie.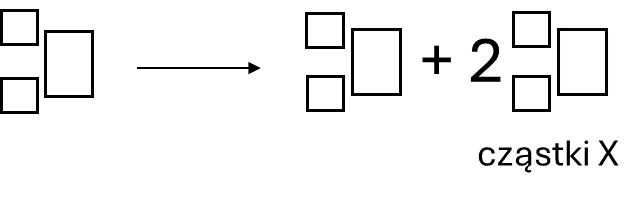
Zadanie 2
Kiedy jądro ma nadmiar protonów, w jego wnętrzu może zajść przemiana β+, w której z protonu powstają neutron, pozyton (e+ lub β+) i neutrino (ν).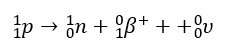
Pozyton jest cząstką różniącą się od elektronu tylko znakiem ładunku elektrycznego. Bezwzględna wartość ładunku oraz masa obydwu cząstek są jednakowe. Neutrino jest nienaładowaną elektrycznie cząstką o masie spoczynkowej bliskiej zeru.
Część jąder atomowych niklu-48 ulega rozpadowi w przemianie β+.
Napisz równanie opisanej przemiany. Uzupełnij wszystkie pola w poniższym schemacie.
Zadanie 3
Jądra atomowe trzeciego nuklidu, który powstaje w wyniku rozpadu niklu-48 ma liczbę masową równą 47. Podczas tego rozpadu emitowane są zarówno cząstki oznaczone jako X, jak i cząstki β+.
Ustal, które cząstki (cząstki oznaczone w zadaniu nr 1 jako X, cząstki β+) i w jakiej liczbie są emitowane podczas opisanej przemiany. Uzupełnij schemat, podaj symbol chemiczny oraz liczbę atomową powstającego nuklidu.Liczba cząstek X: …….
Liczba cząstek β+: …….
Atomy pewnego metalicznego pierwiastka oznaczonego umownie symbolem X występują naturalnie w postaci 5 izotopów o liczbach masowych: 58 (68,077% atomów), 60 (26,233% atomów), 61 (1,14% atomów), 62 (3,634% atomów) oraz 64 (0,926%).
W wyniku analizy pewnej próbki metalu X stwierdzono, że średnia ważona liczb masowych wszystkich atomów jest równa 59,142.
Zadanie 1
Wykonaj odpowiednie obliczenia i rozstrzygnij, czy analizowana próbka jest naturalnie występującą mieszaniną izotopów, czy też jest sztucznie wzbogacona w jeden z izotopów.Rozstrzygnięcie: ……………………….
Zadanie 2
Z podanego zestawu wybierz tę wartość, która przedstawia masę atomową naturalnego pierwiastka X. Podaj jego symbol.
a) 57,935 u
b) 58,693 u
c) 58,766 u
d) 59,142 u
e) 59,452 u
Symbol pierwiastka: ……….Nie uwzględniając izomerii optycznej, wyróżniamy 4 alkohole o wzorze C4H9OH (butylowe). Wszystkie w stanie ciekłym są bezbarwnymi cieczami, ale różnią się właściwościami fizycznymi. W tabeli przedstawiono wzory odpowiednich izomerów i temperatury przemian fazowych pod ciśnieniem 1013 hPa.
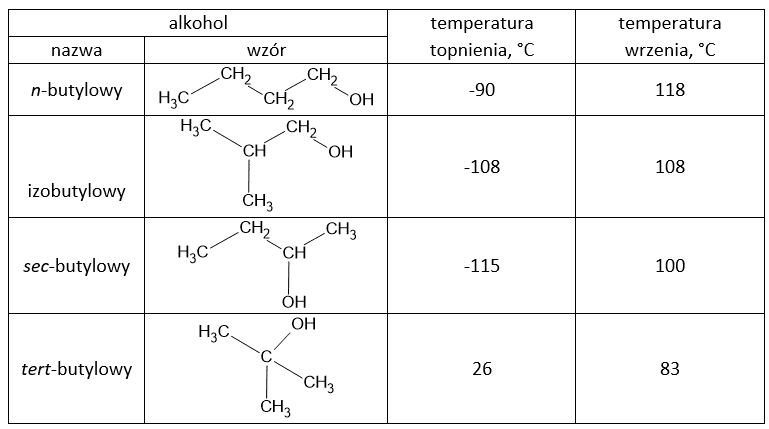
Zadanie 1
W szafce laboratoryjnej przechowywana jest erlenmajerka z jednym z izomerów. Erlenmajerkę po wyjęciu z szafki przedstawiono na fotografii.
Rozstrzygnij, który z alkoholi butylowych jest przechowywany w erlenmajerce. Podaj jego nazwę zwyczajową lub systematyczną. Uzasadnij swój wybór.
Nazwa: …………………………………………………..
Uzasadnienie:..................................................................................
Zadanie 2
Rozstrzygnij, czy zdanie poniżej jest prawdziwe, czy fałszywe. Wybierz i podkreśl jedno określenia z nawiasu i uzasadnij swój wybór.
Z podanych alkoholi najmniej lotny jest alkohol tert-butylowy, ponieważ ma najwyższą temperaturę topnienia.
Rozstrzygnięcie: zdanie jest (prawdziwe / fałszywe).
Uzasadnienie: .......................................................Do 100 g chemicznie czystej wody wsypano 50 g K2SO4 i zamieszano. Rozpuszczalność K2SO4 w temperaturze wykonania doświadczenia wynosi 11,1 g na 100 g H2O.
Zadanie 1:
Oblicz masę kryształów pozostających w równowadze z roztworem nasyconym i stopień dysocjacji K2SO4.
Zadanie 2:
Dokończ zdania. Wybierz po jednym określeniu z każdego nawiasu.
Wprowadzenie do nasyconego roztworu K2SO4 stałego K2CO3 spowoduje zmniejszenie (wydajności dysocjacji / stopnia dysocjacji / rozpuszczalności) K2SO4. Jest to spowodowane wprowadzeniem dodatkowych (jonów K+ / jonów OH- ze względu na hydrolizę). Zjawisko to nosi nazwę (iloczynu rozpuszczalności / efektu wspólnego jonu).
W wyniku całkowitego spalenia pary węglowodoru X otrzymano 7,5 dm3 (w przeliczeniu na warunki normalne) spalin zawierających tylko CO2 i H2O. Po wykropleniu pary wodnej pozostały gaz zajmuje w warunkach normalnych objętość 5 dm3. Gęstość par węglowodoru X jest 3 razy większa niż gęstość etynu (mierzona w identycznych warunkach).
Ustal nazwę węglowodoru X.