Zadania z działu: Chemia nieorganiczna (pierwiastki bloków s, p, d)
Wodorotlenek wapnia jest związkiem trudno rozpuszczalnym w wodzie. W gorącej wodzie jego rozpuszczalność jest nieco niższa niż w zimnej. Związek ten otrzymuje się w egzotermicznej reakcji CaO z wodą. Przeprowadzono doświadczenie, w którym do zlewki z wodą o temperaturze 20 °C wprowadzono stały CaO.
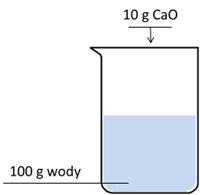
Następnie zamieszano zawartość zlewki.
Zadanie 1.
Nasycony roztwór wodorotlenku wapnia zwiemy wodą wapienną, a wodną zawiesinę tego związku mlekiem wapiennym.
Dokończ zdania. Wybierz i zaznacz jedno określenie spośród podanych w każdym nawiasie.
W opisanym doświadczeniu otrzymano (wodę wapienną / mleko wapienne). Mleko wapienne można otrzymać wprowadzając do wody wapiennej (tlenek wapnia / wodorotlenek wapnia / tlenek lub wodorotlenek wapnia). Wodę wapienną można otrzymać z mleka wapiennego przez wprowadzenie do niego (wody destylowanej / tlenku wapnia ).
Zadanie 2.
Po dodaniu CaO i zamieszaniu zawartości zlewki nie stwierdzono zaniku, ani zmiany barwy ciała stałego.
Wyjaśnij, dlaczego na podstawie powyższej obserwacji nie można zgodzić się ze stwierdzeniem:
Brak widocznych objawów reakcji jest równoznaczny z brakiem reakcji chemicznej.
Odnieś się do stanu układu przed i po zamieszaniu zawartości zlewki.
………………………………………………………………………………………
Zadanie 3.
Z podanych poniżej czynności wybierz te, które należy wykonać, aby potwierdzić, że w opisanym doświadczeniu otrzymano Ca(OH)2. Podkreśl wszystkie prawidłowe czynności.• Wprowadzenie kwasu solnego • Wprowadzenie kropli alkoholowego roztworu fenoloftaleiny • Wprowadzenie zwilżonego uniwersalnego papierka wskaźnikowego u wylotu zlewki • Porównanie temperatury ścianek zlewki przed i po zakończeniu doświadczenia • Dodatek zasady sodowej
Zadanie 4.
Oceń, czy podane poniżej informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.1.
W tej samej temperaturze mleko wapienne ma wyższe pH niż woda wapienna ze względu na wyższy udział Ca(OH)2.
P
F
2.
Ogrzewając wodę wapienną bez dostępu powietrza zaobserwujemy wytrącenie nieznacznej ilości osadu Ca(OH)2.
P
F
3.
Woda wapienna służy do wykrywania CO2 w powietrzu lub innych gazach. Zamiast niej można użyć mleka wapiennego.
P
F
W 20 °C rozpuszczalność Na2CO3 i NaHCO3 (w 100 g wody) wynosi odpowiednio 21,5 i 9,6 g. W temperaturze 20 °C przygotowano nasycony roztwór Na2CO3 przez rozpuszczenie 1 mola Na2CO3 w odpowiedniej ilości wody. Następnie, w zestawie uniemożliwiającym opuszczanie układ przez wodę na drodze parowania, przez roztwór przepuszczano gazowy CO2, aż przyrost masy zawartości naczynia wyniósł 44 g. Wydzielony krystaliczny osad odsączono i wysuszono. Wszystkie operacje wykonano nie zmieniając temperatury. Podczas przepuszczania CO2 przez roztwór zaszła reakcja, której równanie przedstawiono poniżej.
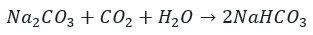
Zadanie 1
Oblicz wydajność otrzymywania NaHCO3 opisaną metodą. Załóż, że masa otrzymanego suchego NaHCO3 otrzymanego po odsączeniu i wysuszeniu ciała stałego jest równa masie wydzielonych kryształów. Przyjmij masy molowe: Na2CO3 – 106 g·mol-1, NaHCO3 – 84 g·mol-1, CO2 – 44 g·mol-1. Wynik podaj w procentach z dokładnością do jedności.Zadanie 2
Rozstrzygnij, czy prawdziwe jest poniższe stwierdzenie. Wybierz i podkreśl rozstrzygnięcie z podanych w nawiasie i uzasadnij swój wybór.
Twierdzenie: otrzymana masa kryształów świadczy o tym, że reakcja pomiędzy roztworem węglanu sodu a tlenkiem węgla(IV) zaszła w mniej niż 80%.
Twierdzenie (jest / nie jest) prawdziwe, ponieważ
……………………………………………………………………………………………………
BaSO4 jest związkiem praktycznie nierozpuszczalnym w wodzie (0,0003 g/100 g wody w 25 °C). Strącono osad BaSO4 przez zmieszanie równych objętości roztworów BaCl2 i Na2SO4 o stężeniu 0,5 mol/dm3 w obu przypadkach. Objętość użytego roztworu BaCl2 wynosiła 0,25 dm3. Po opadnięciu osadu na dno ciecz zdekantowano, a osad zadano porcją 200 cm3 chemicznie czystej wody, zamieszano i ponownie zdekantowano. Płukanie osadu chemicznie czystą wodą wykonywano tak długo, aż w zdekantowanej cieczy nie obserwowano zmętnienia po zmieszaniu z wodnym roztworem AgNO3. Wtedy osad wysuszono. Stwierdzono, że jego masa wynosi 28,80 g.
Zadanie 1
Oblicz wydajność, z jaką otrzymano BaSO4 oraz masę NaCl w mieszaninie poreakcyjnej.
Zadanie 2
Podaj nazwę substancji odpowiedzialnej za zmętnienie powstające po zmieszaniu dekantowanej cieczy z roztworem AgNO3.Do odpowiednio przystosowanego naczynia zawierającego 100 g wody wrzucono 20 g potasu. Nastąpiła reakcja, podczas której uwalnia się ciepło, a faza stała uległa roztworzeniu. Podczas doświadczenia zbierano wodór, a na podstawie jego objętości stwierdzono, że otrzymano go z wydajnością 70%. Doświadczenie przeprowadzono tak, by woda ogrzana ciepłem reakcji nie opuszczała układu w postaci pary wodnej.
Oblicz stężenie procentowe otrzymanego roztworu oraz objętość zebranego wodoru (w warunkach normalnych).Siarczany(VI) tworzą dwie grupy soli podwójnych. Ałuny to sole o wzorze ogólnym:
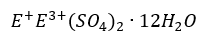
gdzie E+ oznacza kation jednododatni, E3+ kation trójdodatni. Drugą grupą soli podwójnych są sole Tuttona o wzorze ogólnym:
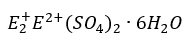
których przedstawicielem jest (NH4)2Fe(SO4)2·6H2O tworzący duże jasnozielone kryształy. Małe kationy litu nie tworzą tego typu soli podwójnych. Aby otrzymać czystą sól podwójną wystarczy rozpuścić w wodzie sole pojedyncze odpowiednim stosunku molowym i pozostawić do odparowania rozpuszczalnika.
Z podanego zestawu wybierz i podkreśl symbole tych metali, których kationy mogą tworzyć zarówno ałuny jak i sole Tuttona.
K, Cr, Mn, Fe, Zn, Al, Pb
Zadanie konkursowe
Wodorotlenek wapnia należy do związków o nieznacznej rozpuszczalności w wodzie, a można go otrzymać w reakcji różnych substancji chemicznych z wodą. Do 4 zlewek wprowadzono po 50 cm3 wody dejonizowanej. Następnie wykonano doświadczenie wg schematu:
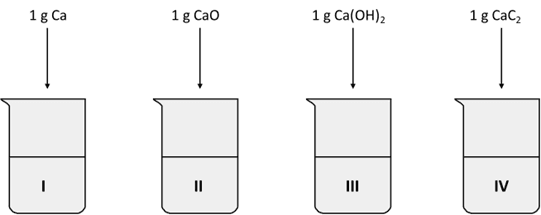
Następnie zawartość zlewek doprowadzono do temperatury 25 °C i porównano pH cieczy. Końcowa objętość fazy ciekłej była identyczna we wszystkich zlewkach.
Zadanie 1
Uszereguj zlewki w kolejności od najmniejszej do największej masy Ca(OH)2 po zakończeniu zmian.Zadanie 2
Uszereguj zlewki w kolejności od najmniejszej do największej wartości pH lub jeśli zwartość zlewek nie różni się pH, to uzasadnij przyczynę tego.We wszystkich zlewkach osiągnięto identyczne pH. Wodorotlenek wapnia w 25 °C rozpuszcza się w ilości ok. 0,16 g/100 g wody. Oznacza to, że w każdej zlewce postał roztwór nasycony i pewna ilość osadu Ca(OH)2 na dnie. We wszystkich zlewkach pH jest więc identyczne.
Zadanie konkursowe
Laboratoryjna metoda otrzymywania wody amoniakalnej polega na wyparciu amoniaku z soli amonowych, a następnie, wykorzystując jego dobre i szybkie rozpuszczanie się w wodzie – na skierowaniu strumienia gazu nad wodę. Przygotowano wodny roztwór NH4NO3, zawiesinę Ca(OH)2 (mleko wapienne) i wodę destylowaną. Następnie zestawiono aparaturę jak na obrazku. Wydzielający się w reakcji amoniak rozpuszczano w wodzie destylowanej.
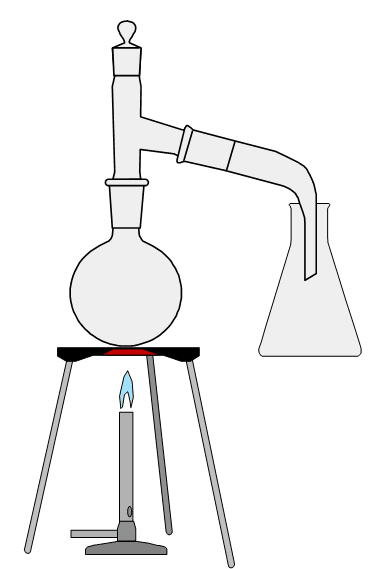
Zadanie 1
Dokończ zdanie. Wpisz wzory lub nazwy substancji w puste miejsca.
Aby otrzymać wodę amoniakalną w kolbie kulistej należy umieścić ..................................... i ...................................., a w kolbie stożkowej należy umieścić ........................................................ .
Zadanie 2
Napisz w postaci cząsteczkowej równanie reakcji zachodzącej podczas otrzymywania gazowego amoniaku opisaną metodą.Zadanie 3
Wyjaśnij, dlaczego poziom cieczy w kolbie stożkowej powinien być tak dobrany, aby rurka wylotowa nie była w niej zanurzona.Zadanie 4
Napisz, jakie dwa objawy możliwe do zaobserwowania świadczą o tym, że w kolbie kulistej ma miejsce reakcja chemiczna.Zadanie 2
Kwas ortofosforowy(V) o wzorze H3PO4 jest ostatecznym i trwałym produktem uwodnienia dekatlenku tetrafosforu. Znanych jest jednak wiele kwasów fosforowych i ich soli. Kwasy takie są produktami częściowego uwodnienia dekatlenku tetrafosforu. Kwas difosforowy(V), zwany także pirofosforowym(V) ma wzór H4P2O7.Związek ten rozpuszczony w wodzie jest kwasem Broensteda, a ujemne logarytmy poszczególnych stałych równowagi dysocjacji (w 25 °C) mają następujące wartości: pKa1 = 0,91, pKa2 = 2,10, pKa3 = 6,70, pKa4 = 9,32.
Zadanie 2.1
Oceń poprawność zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli jest fałszywa.H4P2O7 jest kwasem słabszym od H3PO4
P
F
H4P2O7 jest kwasem czteroprotonowym
P
F
Zadanie 2.2
Difosforany(V) można otrzymać w wyniku ogrzewania wodorofosforanów(V), np.: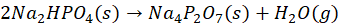
Difosforan(V) sodu jak i kwas disfosforowy są dobrze rozpuszczalne w wodzie. Cechą charakterystyczną takich roztworów jest ich nietrwałość. W roztworach tych dochodzi do powolnej reakcji z wodą, o czym świadczą zmiany pH tych roztworów (pomiary wykonywane w tej samej temperaturze).
a) Napisz w postaci cząsteczkowej równanie reakcji kwasu difosforowego(V) z wodą.
b) Napisz w postaci jonowej równanie reakcji anionów difosforanowych(V) z wodą.
Zadanie R1
Przygotowano zestaw 2 probówek, w których (w nieznanej kolejności) umieszczono roztwór wodorosiarczanu(IV) sodu w wodzie oraz roztwór siarczanu(IV) sodu w wodzie.Do obu probówek wprowadzoną po kilka kropel roztworu KMnO4. Zanotowano następujące zmiany:
I – powstanie brunatnej zawiesiny, po opadnięciu osadu ciecz nad nim jest bezbarwna
II – powstanie bezbarwnego roztworu
Napisz wzory soli, które znajdowały się w poszczególnych probówkach.
Probówka I:…………………………………………………..
Probówka II:………………………………………………….