Zadania z działu: Chemia nieorganiczna (pierwiastki bloków s, p, d)
W temperaturze 0 °C rozpuszczalność stałego jodku sodu w ciekłym SO2 wynosi 15 g na 100 g rozpuszczalnika. W tych warunkach w równowadze z roztworem nasyconym są kryształy o wzorze NaI·4SO2.
Przygotowano 200 g roztworu jodku sodu w ciekłym SO2, nasyconego w temperaturze 0 °C. Roztwór przechowywano w szczelnie zamkniętej ampule w temperaturze 0 °C. Po pewnym czasie ostrożnie otwarto ampułę, co poskutkowało odparowaniem części rozpuszczalnika i wydobywaniem się gazowego SO2 na zewnątrz. Ampułę zamknięto po kilku minutach i stwierdzono, że masa jej zawartości spadła o 20 g. Ampułę ponownie umieszczono w temperaturze 0 °C i pojawiły się w niej kryształy.Zadania 1
Oblicz masę wydzielonych kryształów.Zadania 2
Podaj stężenie (w procentach masowych) roztworu nad wydzielonymi kryształami.Zadania 3
Dokończ zdania. Wybierz po jednym określeniu z każdego nawiasu. Uzasadnij wybór.Należy się spodziewać, że w temperaturze 0 °C rozpuszczalność NaI w ciekłym CO2 jest (na zbliżonym poziomie jak w / znacznie niższa niż / znacznie wyższa niż) w ciekłym SO2. Wynika to z faktu, że CO2 jest rozpuszczalnikiem …………………………… a SO2 jest rozpuszczalnikiem …………………………. . Różny charakter CO2 i SO2 jako rozpuszczalników wynika z różnicy w budowie ich cząsteczek. Cząsteczka SO2 ma kształt (liniowy / kątowy / piramidy trygonalnej), a cząsteczka CO2 ma kształt (liniowy / kątowy / piramidy trygonalnej).
Zadanie R10
Poniżej przedstawiono wzory stereochemiczne różnych tlenków fosforu.
a) Podaj wszystkie symbole, którymi oznaczono wzory tlenków mieszanych.....................................................................
b) Dokończ zdanie. Wybierz jedno określenie z nawiasu i napisz, ile moli elektronów jest wymienianych we opisanym procesie.
W procesie przekształcenia 2 moli związku A w związek C, związek A formalnie (oddaje / pobiera) …… moli elektronów.
Zadanie R6
Siarczan(IV) amonu jest solą dobrze rozpuszczalną w wodzie. Ze względu na podatność anionu na utlenianie – roztwory takie nie są trwałe, jeśli są wystawione na działanie powietrza. Odczyn roztworu siarczanu(IV) amonu można jednoznacznie potwierdzić za pomocą błękitu bromotymolowego.Zadanie R6.1
Na podstawie odpowiednich danych ustal odczyn wodnego roztworu siarczanu(IV) amonu w temperaturze 25 °C. Napisz, jaką barwę przyjmie błękit bromotymolowy w roztworze tej soli.Odczyn: ……………………………
Barwa wskaźnika: …………………………Zadanie R6.2
Do probówki wprowadzono 5 cm3 wodnego roztworu siarczanu(IV) amonu o stężeniu 0,2 mol/dm3 i dodano kilka kropel roztworu wskaźnika. Następnie wprowadzono 1 cm3 roztworu nadtlenku wodoru o stężeniu 1 mol/dm3.
Napisz w formie jonowej skróconej równanie reakcji utleniania, która zaszła po wprowadzeniu roztworu nadtlenku wodoru. Podaj barwę roztworu po zakończeniu reakcji chemicznej.Równanie reakcji utleniania: ……………………………………
Barwa wskaźnika po zakończeniu reakcji chemicznej: …………………………………………….
Zadanie R5
Po zmieszaniu wodnego roztworu azotanu(V) srebra(I) z wodnym roztworem nadtlenodisiarczanu potasu dochodzi do wytrącenia brunatnoczarnego osadu. Schemat reakcji przedstawiono poniżej.
AgNO3 + K2S2O8 + H2O → Ag4O4 + KHSO4 + HNO3
Zadanie R5.1
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie.
Równanie redukcji:………………..
Równanie utleniania:……………..
Zadanie R5.2
Związek o wzorze Ag4O4 ma bardzo silne właściwości utleniające. Potraktowany stężonym kwasem azotowym roztwarza się tworząc roztwór o intensywnej barwie brunatnej. W roztworze tym srebro istnieje w postaci dwudodatnich kationów. Po rozcieńczeniu tego roztworu w wodzie ponownie strąca się Ag4O4.
Napisz w postaci cząsteczkowej równanie reakcji zachodzącej po wprowadzeniu stałego Ag4O4 do stężonego kwasu azotowego(V) (równanie I) oraz po rozcieńczeniu otrzymanego roztworu w wodzie (równanie II).Równanie I: ………………..
Równanie II: …………….....
Zadanie R5.3
Na podstawie przedstawionych informacji określ trwałość kationów srebra w wodnym środowisku w zależności od stopnia utlenienia. Dokończ zdania. Wybierz i podkreśl jedną z odpowiedzi z podanych w nawiasach.
Kationy Ag+ są (trwałe / nietrwałe) w wodnym środowisku.
Kationy Ag2+ są (trwałe / nietrwałe) w wodnym środowisku.
Zadanie R4
Napisz w formie jonowej skróconej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równanie reakcji utleniania i równanie reakcji utleniania zachodzących podczas przemiany widocznej na schemacie. Napisz w formie jonowej skróconej sumaryczne równanie reakcji utleniania i redukcji.
a) S2O32- + I2 → S4O62- + I-
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___S2O32- + ___I2 → ___S4O62- + ___I-
b) Ag4O4 + Sn2+ + H+ → Ag + Sn4+ + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Ag4O4 + ___Sn2+ + ___H+ → ___Ag + ___Sn4+ + ___H2O
c) PbO2 + Mn2+ + H+ → Pb2+ + MnO4- + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___PbO2 + ___Mn2+ + ___H+ → ___Pb2+ + ___MnO4- + ___H2O
d) Zn + NO3- + H+→ Zn2+ + NH3OH+ + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Zn + ___NO3- + ___H+→ ___Zn2+ + ___NH3OH+ + ___H2O
e) Cu2O + [Ag(NH3)2]+ + H2O → [Cu(NH3)4]2+ + Cu(OH)2 + Ag
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___Cu2O + ___[Ag(NH3)2]+ + ___H2O → ___[Cu(NH3)4]2+ + ___Cu(OH)2 + ___Ag
f) [Cr(OH)6]3- + [Ag(NH3)2]+ + OH- → CrO42- + Ag + NH3 + H2O
Równanie redukcji:………………...................................
Równanie utleniania:……………...................................
Sumaryczne równanie reakcji utleniania i redukcji:
___[Cr(OH)6]3- + ___[Ag(NH3)2]+ + ___2OH- → ___CrO42- + ___Ag + ___NH3 + ___H2O
Zadanie 4
Przeprowadzono dwuetapowe doświadczenie. Pierwszy etap przedstawiono poniżej:
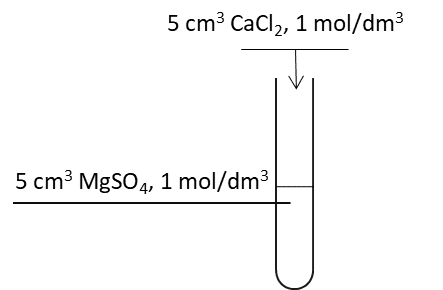
Zaobserwowano powstanie białego osadu. Zawiesinę przesączono. W etapie II do 5 cm3 przesączu dodano 5 cm3 roztworu BaCl2 o stężeniu 1 mol/dm3.
Napisz równanie reakcji zachodzącej w etapie II lub napisz, że reakcja nie zachodzi.
Tlenek wapnia w sposób egzotermiczny reaguje z wodą wg równania:
CaO + H2O → Ca(OH)2
Przeprowadzono dwa doświadczenia, przedstawione na schemacie. Wszystkie składniki oraz otoczenie miały początkową temperaturę 25 °C. Temperatura otoczenia nie zmieniła się podczas doświadczenia.
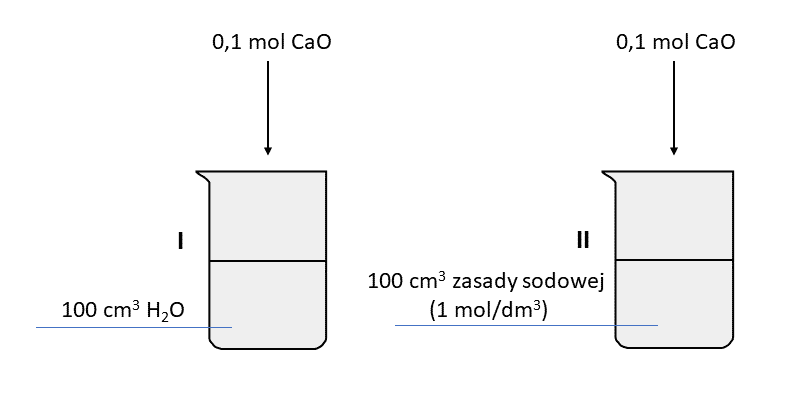
Zadanie 1
Uzupełnij zdania. Wybierz i podkreśl po jednym określeniu z nawiasu.
Po zamieszaniu zawartości temperatura układu w zlewce I była (wyższa od 25 °C / niższa od 25 °C), co oznacza, że układ (zaczął oddawać ciepło do otoczenia / przyjmować ciepło od otoczenia). Po zakończeniu zmian w zlewce I otrzymano (układ jednorodny / zawiesinę).Zadanie 2
W zlewce II zaobserwowano powstanie zawiesiny.
Wybierz zdanie, które w prawidłowo opisuje wynik doświadczenia w zlewce II.
A. W zlewce II nie doszło do zmiany temperatury, ponieważ tlenek wapnia nie reaguje z zasadą sodową.
B. Otrzymanie zawiesiny świadczy o tym, że tlenek wapnia nie reaguje z zasadą sodową.
C. W zlewce II zaszła reakcja, ale jej substraty i produkty są inne niż w zlewce I, więc efekt cieplny jest inny niż w zlewce I. Powstanie zawiesiny nie świadczy o braku reakcji w zlewce II.
D. Tlenek wapnia przereagował z zasadą sodową, a efekt cieplny jest praktycznie taki sam jak w zlewce I. Powstanie zawiesiny nie świadczy o braku reakcji w zlewce II.
Zadanie z kwasem mrówkowym i próbą Trommera, jakie mogłoby pojawić się na maturze 😊
Przypominam też, że NIE MUSICIE WIEDZIEĆ, CZY KWAS MRÓWKOWY ULEGA PRÓBIE TROMMERA ALBO TOLLENSA. MACIE TYLKO WIEDZIEĆ, ŻE KWAS TEN MA (WOBEC SILNYCH UTLENIACZY) WŁAŚCIWOŚCI REDUKUJĄCE. Dalsze informacje dla tegorocznych maturzystów znajdują się pod treścią zadania.
Przeprowadzono serię doświadczeń, w których porównywano zachowanie dwóch reduktorów organicznych: metanalu i kwasu metanowego (mrówkowego) wobec różnych utleniaczy w wodnym środowisku: roztwór wodorotlenku diaminasrebra i zalkalizowana zawiesina wodorotlenku miedzi(II). W doświadczeniach nr 4 i 5 użyto takiej ilości zasady, by dodany kwas metanowy nie spowodował zmiany odczynu mieszaniny reakcyjnej na obojętny lub kwasowy. Wyniki doświadczenia przedstawiono w tabeli. Pewne miejsce pozostawiono jednak puste, a w pozostałych przypadkach podano niektóre z objawów reakcji.
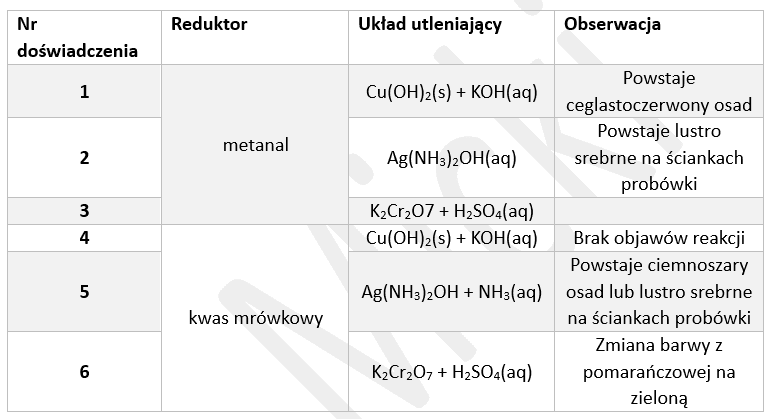
Uzupełnij poniższe zdania. Wybierz i podkreśl jedno wyrażenie z podanych w nawiasach.
Można stwierdzić, że metanal ma (silniejsze / słabsze) właściwości redukcyjne, niż kwas metanowy. W zasadowym środowisku, spośród Cu(OH)2(s) i [Ag(NH3)2]+ silniejszym utleniaczem jest ten (pierwszy / drugi). Na podstawie wyniku doświadczenia nr 6 można stwierdzić, że roztwór reakcyjny w doświadczeniu nr 3 (pozostał pomarańczowy / zmienił barwę z pomarańczowej na żółtą / zmienił barwę z pomarańczowej na zieloną). Uwalnianie się bezbarwnego gazu zaobserwowano w doświadczeniu nr 6. Gaz ten (powstawał także / nie powstawał) w doświadczeniu nr 5.
********************************************
W 2015 roku pojawiło się zadanie dotyczące zachowania kwasu mrówkowego w próbie Trommera. Z INFORMACJĄ WSTĘPNĄ, bo jak piszę - nigdy nie było w wymaganiach, by znać zachowanie tego kwasu w próbie Trommera czy Tollensa. Takie zadanie już więcej się nie pojawiło, ponieważ:
w CKE juz od dawna wiedzą, że kwas ten nie ulega próbie Trommera,
dawniej maturę przygotowywano na podstawie informacji z podręczników szkolnych (którymi zresztą żyje większość chemików). Obecnie treści te są bardziej weryfikowane i jest coraz mniej bubli na maturze, a pewnych rzeczy NIE MA JUŻ WCALE NA maturze z chemii. Bo wiadomo, że były błędne, że pewne rzeczy w podręcznikach są błędne. I nie jest ich mało,
informacja do zadania z 2015 była błędna: oparta na podręcznikowych przekłamaniach, ponadto opis był niezgodny z procedurą przeprowadzania próby Trommera - taki jak do dziś serwują podręczniki szkolne,
Jeśli sami porównacie nowsze i starsze arkusze, to sami zauważycie sporą różnicę w opisach próby Trommera i Tollensa w treści zadań.
No dobra, ale to, że zadanie z 2015 roku było bublem i więcej takowego nie będzie. Ale to nie oznacza, że o ten kwas w ogóle nie będą pytać. Że nie będzie jakiegoś redoksa albo czegoś innego z tym kwasem. Rok temu wymyśliłem takie zadanie, które ma pokazać, jakich zadań co do HCOOH możnaby się spodziewać po skorygowaniu wiadomości co do zachowania się HCOOH.
To, że się dowiedzieli o tym, że HCOOH nie ulega próbie Trommera nie spowodowało, że system egzaminowania padł, a w CKE wszyscy poszli z torbami. Nie po raz pierwszy informacja dotycząca czegoś nie pokrywa się z jakimś starszym arkuszem. Dlatego uważam, że ze zbiorów zadań bazujących na kopiuj+wklej z arkuszy CKE należy pewne zadania powywalać, bo dziś wprowadzają w błąd i są źródłem zamieszania. Tak więc to, że raz palnęli: "HCOOH ulega próbie Trommera" nie oznacza, że "na maturze piszemy, że HCOOH ulega próbie Trommera". A co zrobicie, jak serio dostaniecie takie zadanie podobne do tego? Odpowiecie sprzecznie z podaną infomacją do zadania, bo na maturze piszemy że... Czy raczej wywnioskujecie coś z tej informacji?
A jeśli ktoś będzie miał zagwozdkę "dlaczego takie odpowiedzi?" to niech sobie spróbuje zapisać równanie albo chociaż schemat reakcji - z uwzględnieniem środowiska, w którym ta reakcja zachodzi ☺
Przeprowadzono doświadczenie zilustrowane poniższym schematem.
Celem doświadczenia było odróżnienie dwóch, oznaczonych umownie literami X i Z, metali, z których wykonano płytki. Wiadomo, że jednym metalem był cynk, a drugim – nikiel.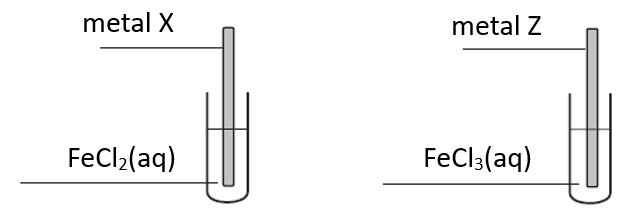
Po pewnym czasie płytki wyjęto z roztworów i osuszono. Zważono płytkę wykonaną z metalu X i stwierdzono, że masa tej płytki uległa zmianie.
Zadanie 1
Uzupełnij poniższe zdania. Wybierz i zaznacz właściwe określenie spośród podanych w każdym nawiasie oraz napisz w formie jonowej skróconej równanie zachodzącej reakcji.
Masa płytki wykonanej z metalu X się (zmniejszyła / zwiększyła), a podczas przeprowadzonego doświadczenia przebiegła reakcja zilustrowana równaniem:
.................................................................................................
Metalem Z był (cynk / nikiel).
Zadanie 2
Rozstrzygnij, czy do odróżnienia metali od siebie wystarczająca jest informacja, że masa płytki wykonanej z metalu X uległa zmianie. Wybierz po jednym określeniu z każdego nawiasu.
Odróżnienie metali na podstawie tej informacji (jest / nie jest) możliwe, ponieważ w czasie trwania doświadczenia masa płytki wykonanej z metalu Z się (także się zmniejszyła / także się zwiększyła / nie uległa zmianie). W naczyniu, w którym umieszczona była płytka z metalu Z (sól żelaza pozostała niezmieniona / powstała inna sól żelaza / powstało metaliczne żelazo).
Ciekły (skroplony) amoniak (NH3(c)) jest rozpuszczalnikiem, który – podobnie jak woda – ulega autodysocjacji
polegającej na przeniesieniu protonu między cząsteczkami rozpuszczalnika, w wyniku czego powstają forma kationowa oraz forma anionowa rozpuszczalnika.
NH3 + NH3 ⇄ NH4++ NH2-
Ciekły amoniak jest rozpuszczalnikiem dla wielu polarnych związków. Te substancje, które rozpuszczone w amoniaku powodują zwiększenie stężenia formy kationowej, są w danym rozpuszczalniku kwasami, a te, które zwiększają stężenie formy anionowej, są w danym rozpuszczalniku zasadami.Zadanie 1
Chlorowodór po rozpuszczeniu w ciekłym amoniaku tworzy mocny elektrolit.
Zapisz równanie dysocjacji chlorowodoru w ciekłym amoniaku. Uwzględnij, że w procesie tym powstaje odpowiednia forma rozpuszczalnika. Napisz, jaki jest odczyn otrzymanego roztworu (kwasowy, obojętny lub zasadowy).Równanie reakcji:…………………………………………….
Odczyn roztworu:………………………………………….Zadanie 2
Azotan(V) amonu rozpuszcza się w ciekłym amoniaku. Roztwór utleniająco na metale, podobnie jak roztwór HNO3 w wodzie. W przypadku miedzi reakcję z roztworem NH4NO3 w amoniaku przedstawia schemat:
Cu + NH4++ NO3- → Cu2+ + NO2- + H2O + NH3
Do amoniakalnego roztworu NH4NO3 w NH3(c) wprowadzono (w nadmiarze) metaliczną miedź. Reakcja zaszła w 100%.
Oceń poprawność poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa albo F, jeśli jest fałszywa.
W reakcji metalicznej miedzi z roztworem NH4NO3 w NH3(c) powstaje brunatny gaz
P
F
Rozpuszczając w skroplonym amoniaku NH4NO3 można otrzymać roztwór o tych samych właściwościach, co rozpuszczając HNO3 w skroplonym amoniaku.
P
F
W mieszaninie poreakcyjnej obecne są związki azotu(-III), azotu(III) i azotu(V).
P
F