Zadania z działu: Prawa gazowe
Wszystkie umieszczone tutaj zadania są autorskie i nie mogą być udostępniane w innych opracowaniach/materiałach, umieszczane na innych witrynach internetowych bez wcześniejszej wiedzy i zgody autora.W 20 °C pod ciśnieniem normalnym (1013 hPa) rozpuszczalność gazowego amoniaku w wodzie wynosi 40 g/100 cm3 wody.
Zadanie 1
Oblicz, jaką objętość w podanych warunkach zajmował amoniak, który rozpuszczono w 100 cm3 wody otrzymując roztwór nasycony.Zadanie 1
Podaj w jakim stosunku objętościowym miesza się gazowy amoniak z wodą w podanych warunkach.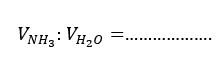
Zadanie 1
Poprawna odpowiedź:
40 g NH3 → 2,353 mol → 56,6 dm3
Zadanie 1
Poprawna odpowiedź: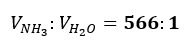
W dwóch pojemnikach o stałej objętości 2 dm3 znajdowały się gazy o temperaturze 20 °C i pod ciśnieniem 1013 hPa. W pierwszym: azot, w drugim: amoniak. Następnie do każdego naczynia wpompowano po 1 dm3 ciekłej wody o tej samej temperaturze. Otrzymano układ jak na przedstawionym obrazku.
Po pewnym czasie dokonano pomiaru ciśnienia w obu zbiornikach. Stwierdzono, że w jednym zbiorniku ciśnienie jest blisko 2 razy wyższe od 1013 hPa, a w drugim – spadło znacznie poniżej 1013 hPa, podczas gdy temperatura w obu zbiornikach nie uległa zmianie względem pierwotnej wartości.
Zadanie 1
Napisz, jaki gaz był zawarty w zbiorniku, w którym zaobserwowano znaczny spadek ciśnienia. Uzasadnij swój wybór.Zadanie 2
Tylko w jednym ze zbiorników zaobserwowano wielokrotny wzrost przewodnictwa elektrycznego fazy ciekłej. Napisz równanie równowagowego procesu odpowiedzialnego ten fakt.Zadanie 1
Poprawna odpowiedź:Spośród N2 i NH3 tylko ten drugi dobrze rozpuszcza się w wodzie, podczas gdy azot jest bardzo słabo rozpuszczalny w wodzie. W zbiorniku z NH3 liczba cząsteczek gazu nad cieczą znacznie się zmniejszy wskutek rozpuszczania co pociągnie za sobą spadek ciśnienia.
Zadanie 2
Poprawna odpowiedź: