Zadania z działu: Mikołajkowe rozdanie
Wszystkie umieszczone tutaj zadania są autorskie i nie mogą być udostępniane w innych opracowaniach/materiałach, umieszczane na innych witrynach internetowych bez wcześniejszej wiedzy i zgody autora.Zadanie 1
Kwas cytrynowy (kwas 2-hydroksypropano-1,2,3-trikarboksylowy) poddany działaniu wodnego roztworu KMnO4 ulega reakcji, w której zostaje przekształcony w kwas acetono-1,3-dikarboksylowy. Jednocześnie obserwuje się powstanie brunatnej zawiesiny i uwalnianie bezbarwnego gazu. Ciało stałe usuwa wprowadzając roztwór szczawianu amonu oraz rozcieńczony roztwór H2SO4 w wodzie. Na końcu, do bezbarwnego roztworu wprowadza się wodę bromową – powoduje to strącenie praktycznie nierozpuszczalnego w wodzie pentabromoacetonu i wydzielenie bezbarwnego gazu.Napisz w formie jonowej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy), równanie reakcji redukcji i równanie reakcji utleniania, które zaszły podczas opisanej przemiany. Uwzględnij środowisko reakcji. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
a) Po dodaniu roztworu KMnO4 do roztworu kwasu cytrynowego.
Równanie redukcji: …………………………………………………………………………………
Równanie utleniania: .......................................................................................................
b) Po wprowadzeniu roztworu szczawianu amonu i roztworu H2SO4.
Równanie redukcji: ………………………………………………………………………………………..
Równanie utleniania:
c) Po wprowadzeniu wody bromowej.Równanie redukcji: ………………………………………………………………………………………..
Równanie utleniania:
Odpowiedź:
a)
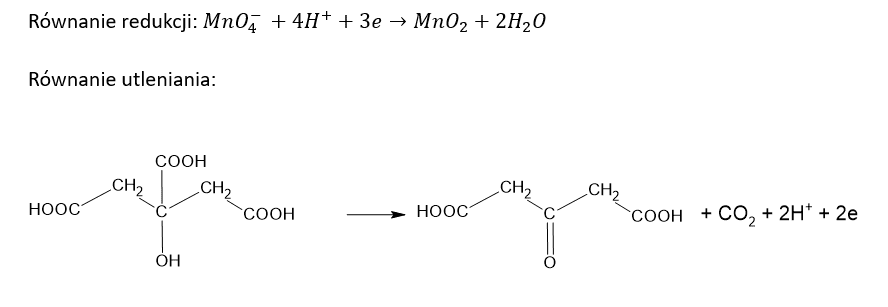
b)
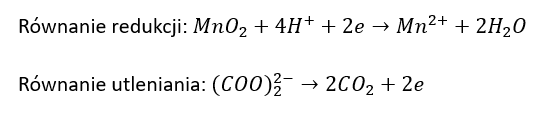
c)
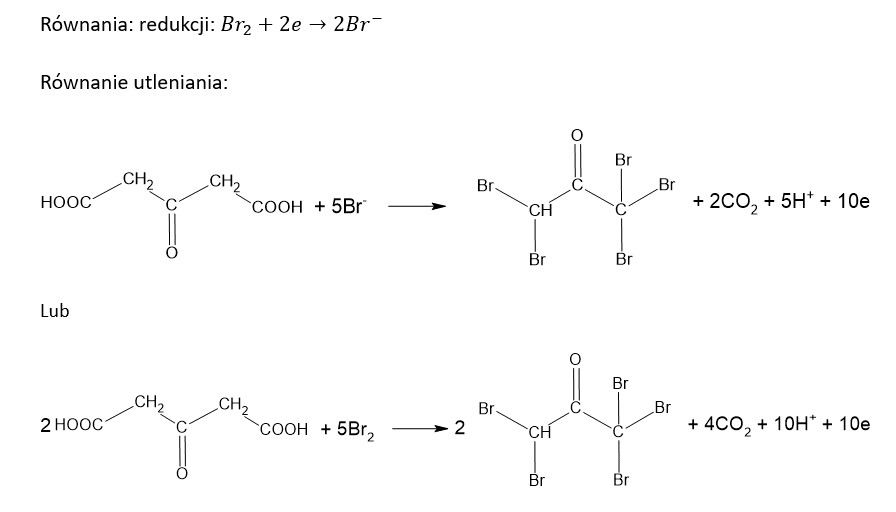
UWAGA: warunkowo dopuszczalne są zapisy z jonami OH- w równaniach reakcji, w których nie uczestniczył mocny kwas.
Zadanie 2
Mieszaniu cieczy towarzyszy zjawisko kontrakcji objętości, czyli zmiana objętości układu. np. w temperaturze pokojowej po wprowadzeniu do jednego naczynia 100 cm3 etanolu i 100 cm3 czystej wody otrzymuje się ok. 194 cm3 roztworu, zamiast spodziewanych 200 cm3.
Wyjaśnij, dlaczego zjawiska zmniejszenia objętości układu nie obserwuje się po umieszczeniu w jednym naczyniu 100 cm3 n-heksanu i 100 cm3 czystej wody.
Odpowiedź:
Woda i n-heksan praktycznie nie mieszają się ze sobą. W związku z tym nie tworzą układu jednorodnego i objętość układu jest sumą objętości obu faz.
Komentarz: to zadanie było najtrudniejsze w ocenianiu, gdyż tylko nieliczne prace jasno wskazywały na niejednorodność układu. Większość odnosiła się do różnic w polarności i braku wiązań wodorowych pomiędzy cząsteczkami wody i n-heksanu. Warunkowo zaliczałem odpowiedzi, które nie wykluczały się z możliwością powstania układu heterogenicznego. Odpowiedzi, które jasno wskazywały na powstanie układu jednorodnego nie były zaliczane.
Zadanie 3
Temperatura krzepnięcia roztworów jest niższa niż temperatura krzepnięcia czystego rozpuszczalnika. Im więcej drobin wprowadzi się do danej masy rozpuszczalnika, tym niższą temperaturę krzepnięcia ma otrzymany roztwór. Zjawisko obniżenia temperatury krzepnięcia w odniesieniu do temperatury krzepnięcia czystego rozpuszczalnika nazywamy efektem krioskopowym.W dwóch zlewkach (oznaczonych jako I i II)znajdowało się po 500 g wody. Następnie do każdej wprowadzono odpowiednią ilość substancji:
Zlewka I – 0,5 mol glukozy
Zlewka II – 0,5 mol sacharozy
Zlewka III – 0,5 mol chlorku sodu
Zlewka IV – 0,5 mol siarczanu(VI) baru
Zawartość każdej zlewki zamieszano. W każdej stwierdzono obecność fazy ciekłej.Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli informacja jest fałszywa.
Roztwór w zlewce II ma niższą temperaturę krzepnięcia niż roztwór w zlewce I, ponieważ sacharoza jest dwucukrem budowanym z glukozy i fruktozy. P F Ciecz w zlewce III ma taką samą temperaturę krzepnięcia, jak ciecz w zlewce IV P F W jednym naczyniu w praktyce nie zaobserwowano efektu krioskopowego P F Odpowiedź:

Komentarz: BaSO4 jest związkiem praktycznie nierozpuszczalnym w wodzie. Z tego powodu efekt krioskopowy jest pomijalny.
Zadanie 4
Przeprowadzono dwuetapowe doświadczenie. Pierwszy etap przedstawiono poniżej:
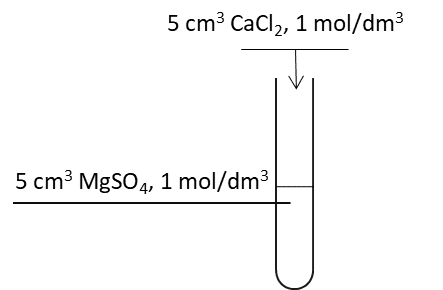
Zaobserwowano powstanie białego osadu. Zawiesinę przesączono. W etapie II do 5 cm3 przesączu dodano 5 cm3 roztworu BaCl2 o stężeniu 1 mol/dm3.
Napisz równanie reakcji zachodzącej w etapie II lub napisz, że reakcja nie zachodzi.
Odpowiedź
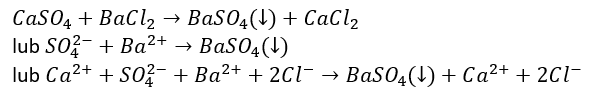
Komentarz: w temperaturze pokojowej rozpuszczalność CaSO4 wynosi ok. 0,25 g/100 g wody. Tzw. woda gipsowa (nasycony roztwór CaSO4) służy do wykrywania jonów Ba2+ strącając osad BaSO4.
Zadanie 5
Poniżej podano efekty energetyczne dwóch reakcji jonowych w stanie standardowym:NaOH(aq) + HCl(aq) → NaCl(aq) + H2O + 55,8 kJ
Ba(NO3)2(aq) + Na2SO4(aq)→ BaSO4(s) + 2NaNO3(aq) + 26,3 kJ
Przeprowadź obliczenia i na podstawie powyższych danych oszacuj standardową entalpię reakcji o podanym równaniu:
Ba(OH)2(aq) + H2SO4(aq) → BaSO4(s) + 2H2O(c)
Odpowiedź
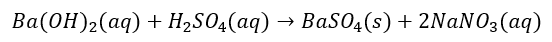
Wartość przybliżona – aby otrzymać poprawny wynik należy jeszcze uwzględnić efekt dysocjacji jonów HSO4- na jony SO42-.
Zadanie 6
Kwas cytrynowy jest kwasem trójprotonowym. Z przesyconych roztworów kwasu cytrynowego (C6H8O7) w wodzie wypadają kryształy o wzorze C6H8O7·xH2O. W celu ustalenia współczynnika x próbkę kryształów o masie 1,211 g (otrzymanych z wodnego roztworu) rozpuszczono w wodzie i miareczkowano roztworem NaOH w obecności fenoloftaleiny. Do pojawienia się trwałego różowego zabarwienia zużyto 69,2 cm3 roztworu NaOH o stężeniu 0,2500 mol/dm3.
Zadanie 6.1
Oblicz wartość współczynnika x.Zadanie 6.2
Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli informacja jest prawdziwa, albo F, jeśli informacja jest fałszywa.
W opisanym hydracie kwasu cytrynowego na jedną cząsteczkę kwasu przypada jedna cząsteczkę wody, a w hydracie o wzorze CuSO4·5H2O na jedną cząsteczkę soli przypada pięć cząsteczek wody. P F Rozpuszczenie w wodzie bezwodnego kwasu cytrynowego i pozostawienie do odparowania wody prowadzi do otrzymania kryształów o wzorze C6H8O7·H2O P F Kwas cytrynowy może reagować z NaOH w stosunku molowym nkwasu : nNaOH = 1 : 1. P F Odpowiedź:
Zadanie 6.1
x = 1
Zadanie 6.2

W przeciwieństwie do kwasu cytrynowego CuSO4 nie jest związkiem cząsteczkowym. Nie można powiedzieć, że w hydracie o wzorze CuSO4·5H2O na jedną cząsteczkę soli przypada pięć cząsteczek wody.