Zadania z działu: Doświadczenia chemiczne
Twój Redoksownik - pobierz wszystkie zadania z reakcjami redoks w jednym pliku do druku.
Zadania R16 i R17
Zadanie R16
Wykonano dwuetapowe doświadczenie. W dwóch probówkach (oznaczonych I i II) znajdowało się po 5 cm3 bezbarwnego wodnego roztworu NaIO4. Do obu probówek wprowadzono niewielką ilość roztworu kwasu askorbinowego (witaminy C) C6H8O6. Zaszła reakcja chemiczna, w wyniku której powstało ciało stałe o ciemnej barwie. W drugim etapie do probówki I wprowadzono kilka cm3 chloroformu i wstrząśnięto zawartością probówki. Wygląd zawartości probówki I po tym etapie przedstawiono poniżej.
Do probówki II wprowadzono dodatkową ilość roztworu kwasu askorbinowego. Nastąpił zanik ciała stałego i powstał bezbarwny roztwór. W obu etapach doświadczenia kwas askorbinowy pełnił tę samą rolę.
a) Zapisz równanie w formie jonowej skróconej równanie reakcji redukcji, która zaszła w pierwszym etapie doświadczenia.
Stwierdzono, że w środowisku zbliżonym do obojętnego w obecności anionów jodanowych(VII) cząsteczka kwasu askorbinowego ulega rozpadowi wg równania, które w uproszeniu można napisać następująco:
C6H8O6 +5H2O ⟶ HCHO + C2O42- + 2HCOO- + CO2 + 14H+ + xe
b)Ustal wartość współczynnika x i napisz stosunek utleniacza do reduktora. Wynik podaj w postaci najmniejszych liczb całkowitych.
x = ….
nutl : nred = …c) zapisz w formie jonowej równanie reakcji odpowiedzialnej za zanik ciała stałego w probówce II. Dokończ zdanie. Wybierz i podkreśl jedną odpowiedź z podanych w nawiasie.
równanie reakcji: ...
W obu etapach doświadczenia wykazano (kwasowe / zasadowe / redukujące / utleniające) właściwości kwasu askorbinowego.
Zadanie R17
Przygotowano probówkę z roztworem KI (probówka I) i probówkę z roztworem KIO3 (probówka II). Oba roztwory są bezbarwne. Do obu probówek wprowadzono po 2 cm3 roztworu Pb(NO3)2. W probówkach nastąpiły zmiany świadczące o zajściu reakcji chemicznej. Efekt doświadczenia przedstawiono na fotografii.Następnie do probówki II wprowadzono 2 cm3 roztworu kwasu askorbinowego i nastąpiły zmiany świadczące o zajściu reakcji chemicznej. Efekt doświadczenia przedstawiono na fotografii.

a) Napisz w formie jonowej skróconej równanie reakcji, które zaszły w probówkach I i II podczas pierwszego etapu doświadczenia.
probówka I: ...
probówka II: ...
b) Napisz w formie jonowej skróconej równanie reakcji redukcji, która zaszła podczas opisanego doświadczenia.
Przygotowano probówkę III, w której umieszczono roztwór KIO3 i nadmiar roztwór kwasu askorbinowego. Probówką wstrząśnięto i wprowadzono kroplę roztworu Pb(NO3)2. Nastąpiło wytrącenie osadu.
c) Napisz, jaki kolor (biały czy żółty) miał wytrącony osad. Podkreśl poprawną odpowiedź z podanych w nawiasie i uzasadnij swój wybór.
Kolor osadu był (biały / żółty).
Uzasadnienie: ....
Zadanie R6
Siarczan(IV) amonu jest solą dobrze rozpuszczalną w wodzie. Ze względu na podatność anionu na utlenianie – roztwory takie nie są trwałe, jeśli są wystawione na działanie powietrza. Odczyn roztworu siarczanu(IV) amonu można jednoznacznie potwierdzić za pomocą błękitu bromotymolowego.Zadanie R6.1
Na podstawie odpowiednich danych ustal odczyn wodnego roztworu siarczanu(IV) amonu w temperaturze 25 °C. Napisz, jaką barwę przyjmie błękit bromotymolowy w roztworze tej soli.Odczyn: ……………………………
Barwa wskaźnika: …………………………Zadanie R6.2
Do probówki wprowadzono 5 cm3 wodnego roztworu siarczanu(IV) amonu o stężeniu 0,2 mol/dm3 i dodano kilka kropel roztworu wskaźnika. Następnie wprowadzono 1 cm3 roztworu nadtlenku wodoru o stężeniu 1 mol/dm3.
Napisz w formie jonowej skróconej równanie reakcji utleniania, która zaszła po wprowadzeniu roztworu nadtlenku wodoru. Podaj barwę roztworu po zakończeniu reakcji chemicznej.Równanie reakcji utleniania: ……………………………………
Barwa wskaźnika po zakończeniu reakcji chemicznej: …………………………………………….
Do probówki ze stałym etanianem (octanem) sodu dodano rozcieńczony kwas solny i zawartość naczynia ogrzano. U wylotu próbówki wyczuwalny był charakterystyczny ostry zapach.
Zadanie 1
Napisz, czy użycie do przeprowadzenia opisanego doświadczenia wodnego roztworu kwasu siarkowego(VI) zamiast kwasu solnego pozwoli na zaobserwowanie podobnych efektów................................................................................................................
Zadanie 2
W dwóch nieopisanych probówkach znajdują się wodne roztwory dwóch soli (każdy roztwór w innej probówce). Wiadomo, że jednym roztworem jest wodny roztwór etanianu (octanu) wapnia, a drugim – wodny roztwór etanianu (octanu) sodu.
Rozstrzygnij, czy po dodaniu wodnego roztworu kwasu siarkowego(VI) do obu probówek i ogrzaniu ich zawartości możliwe będzie wskazanie, w której probówce znajdował się wodny roztwór etanianu wapnia, a w której – wodny roztwór etanianu sodu. Odpowiedź uzasadnij.
Rozstrzygnięcie: ...................................................................................................
Uzasadnienie:………………………………………….................................................Polialkohol winylowy i polietylenoimina są polimerami, których wzory przedstawiono poniżej.
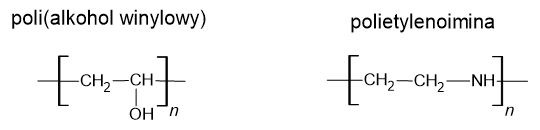
Cechą charakterystyczną obu polimerów jest dobra rozpuszczalność w wodzie. W probówkach oznaczonych numerami I i II znajdują się (w losowej kolejności) roztwory wodne obu polimerów. Roztwór każdego polimeru w osobnej probówce.
Zadanie 1
Zaprojektuj doświadczenie, które pozwoli odróżnić od siebie zawartość probówek. Wpisz nazwę jednego odczynnika wybranego z listy, który wprowadzony do obu probówek pozwoli zidentyfikować roztwory i napisz jaka obserwacja pozwoli odróżnić od siebie roztwory.
a) woda siarkowodorowa, b) alkoholowy roztwór fenoloftaleiny, c) wodny roztwór NaOH, d) woda wapienna
Obserwacja:…………………………………………….
Zadanie 2
Napisz równanie równowagi ustalającej się w wodnym roztworze polimeru, która umożliwia odróżnienie roztworu tego polimeru od roztworu drugiego polimeru wybranym odczynnikiem. W równaniu reakcji użyj fragmentu wzoru łańcucha polimerowego odpowiadający jednemu merowi.
Równanie reakcji:……………………………
Na2SO3 jest solą słabego kwasu z mocną zasadą. W wodnych roztworach dochodzi do hydrolizy anionowej. W probówce przygotowano roztwór Na2SO3 przez zadanie 1 g Na2SO3 wodą destylowaną w ilości 5 cm3 i wstrząśniecie do całkowitego rozpuszczenia się związku.
Z podanego zestawu wybierz i zaznacz wszystkie obserwowane doświadczalnie zjawiska świadczące o równowadze ustalającej się w roztworze tej soli.
a) z roztworu uwalnia się gaz o drażniącym i duszącym zapachu,
b) po dodaniu kropli alkoholowego roztworu fenoloftaleiny do zawartość probówki przyjmuje różowe zabarwienie
c) w probówce wytrąca się galaretowaty biały osad
d) uniwersalny papierek wskaźnikowy umieszczony w roztworze przyjmuje czerwone zabarwienie
Zadanie konkursowe
Wodorotlenek wapnia należy do związków o nieznacznej rozpuszczalności w wodzie, a można go otrzymać w reakcji różnych substancji chemicznych z wodą. Do 4 zlewek wprowadzono po 50 cm3 wody dejonizowanej. Następnie wykonano doświadczenie wg schematu:
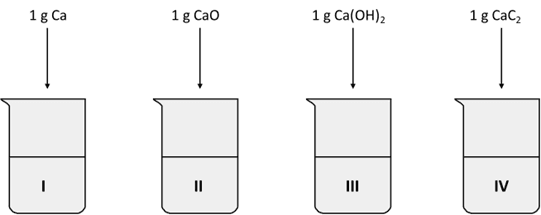
Następnie zawartość zlewek doprowadzono do temperatury 25 °C i porównano pH cieczy. Końcowa objętość fazy ciekłej była identyczna we wszystkich zlewkach.
Zadanie 1
Uszereguj zlewki w kolejności od najmniejszej do największej masy Ca(OH)2 po zakończeniu zmian.Zadanie 2
Uszereguj zlewki w kolejności od najmniejszej do największej wartości pH lub jeśli zwartość zlewek nie różni się pH, to uzasadnij przyczynę tego.We wszystkich zlewkach osiągnięto identyczne pH. Wodorotlenek wapnia w 25 °C rozpuszcza się w ilości ok. 0,16 g/100 g wody. Oznacza to, że w każdej zlewce postał roztwór nasycony i pewna ilość osadu Ca(OH)2 na dnie. We wszystkich zlewkach pH jest więc identyczne.
Zadanie konkursowe
Laboratoryjna metoda otrzymywania wody amoniakalnej polega na wyparciu amoniaku z soli amonowych, a następnie, wykorzystując jego dobre i szybkie rozpuszczanie się w wodzie – na skierowaniu strumienia gazu nad wodę. Przygotowano wodny roztwór NH4NO3, zawiesinę Ca(OH)2 (mleko wapienne) i wodę destylowaną. Następnie zestawiono aparaturę jak na obrazku. Wydzielający się w reakcji amoniak rozpuszczano w wodzie destylowanej.
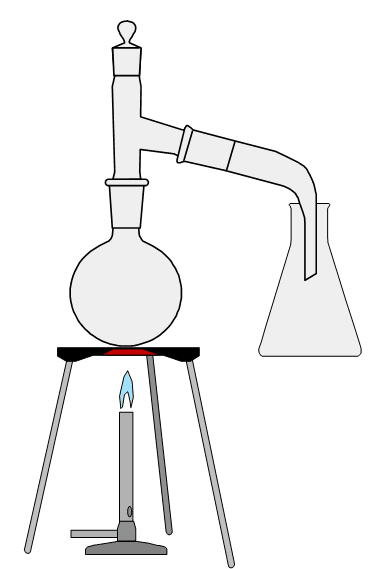
Zadanie 1
Dokończ zdanie. Wpisz wzory lub nazwy substancji w puste miejsca.
Aby otrzymać wodę amoniakalną w kolbie kulistej należy umieścić ..................................... i ...................................., a w kolbie stożkowej należy umieścić ........................................................ .
Zadanie 2
Napisz w postaci cząsteczkowej równanie reakcji zachodzącej podczas otrzymywania gazowego amoniaku opisaną metodą.Zadanie 3
Wyjaśnij, dlaczego poziom cieczy w kolbie stożkowej powinien być tak dobrany, aby rurka wylotowa nie była w niej zanurzona.Zadanie 4
Napisz, jakie dwa objawy możliwe do zaobserwowania świadczą o tym, że w kolbie kulistej ma miejsce reakcja chemiczna.Zadanie R1
Przygotowano zestaw 2 probówek, w których (w nieznanej kolejności) umieszczono roztwór wodorosiarczanu(IV) sodu w wodzie oraz roztwór siarczanu(IV) sodu w wodzie.Do obu probówek wprowadzoną po kilka kropel roztworu KMnO4. Zanotowano następujące zmiany:
I – powstanie brunatnej zawiesiny, po opadnięciu osadu ciecz nad nim jest bezbarwna
II – powstanie bezbarwnego roztworu
Napisz wzory soli, które znajdowały się w poszczególnych probówkach.
Probówka I:…………………………………………………..
Probówka II:………………………………………………….