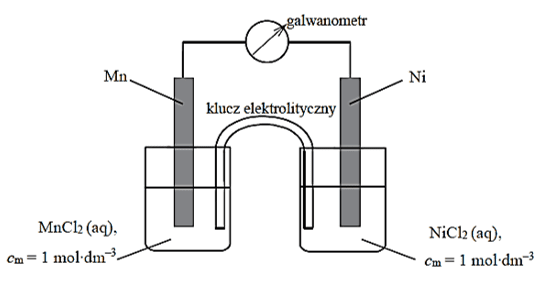
Konwencja sztokholmska
Wśród pytań dotyczących matury z chemii w roku 2024 wiele dotyczy możliwości odwołania w zadaniu 12.1. Wiele osób udzieliło takiej lub podobnej odpowiedzi i odpowiedź uznano za błędną.

Co ciekawe, to takie błędne zapisy można spotkać w odpowiedziach do matury udostępnionych przez różne osoby w Internecie. Wiele osób sugeruje się nimi i jest przekonana, że ich odpowiedź jest poprawna i mogą się od tego odwołać. I szukają kogoś, kto im to odwołanie napisze...
Niestety, ale takie odpowiedzi są nieprawidłowe, a część maturzystów została wprowadzona w błąd i ma złudną wiarę, że ich odpowiedź jest prawidłowa, ale nie została zaliczona ze względu na słynny klucz - trzeba w niego trafić...
Bywają kontrowersyjne przypadki, ale nie tym razem. Wychodzi na to, że od ludzi zdających wymaga się znajomości zapisu schematu ogniw w konwencji sztokholmskiej, ale nie zawsze miały się jak tego nauczyć... Zauważyłem, że to dość pospolita zagwozdka, bo takie pytania:
widzę nie po raz pierwszy. Spójrzmy więc na fragment II części podręcznika "Podstawy obliczeń chemicznych":

Przypadek I - ogniwa z kluczem (mostkiem) elektrolitycznym.
Tak jak pisałem - pytania takie się powielają, więc zawarłem krótko podstawową zasadę w swoim podręczniku. Zwróćmy uwagę na to, że pionowa kreska oznacza granicę faz. W przypadku ogniwa zapisanego schematem:
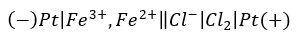
oznacza to tyle:
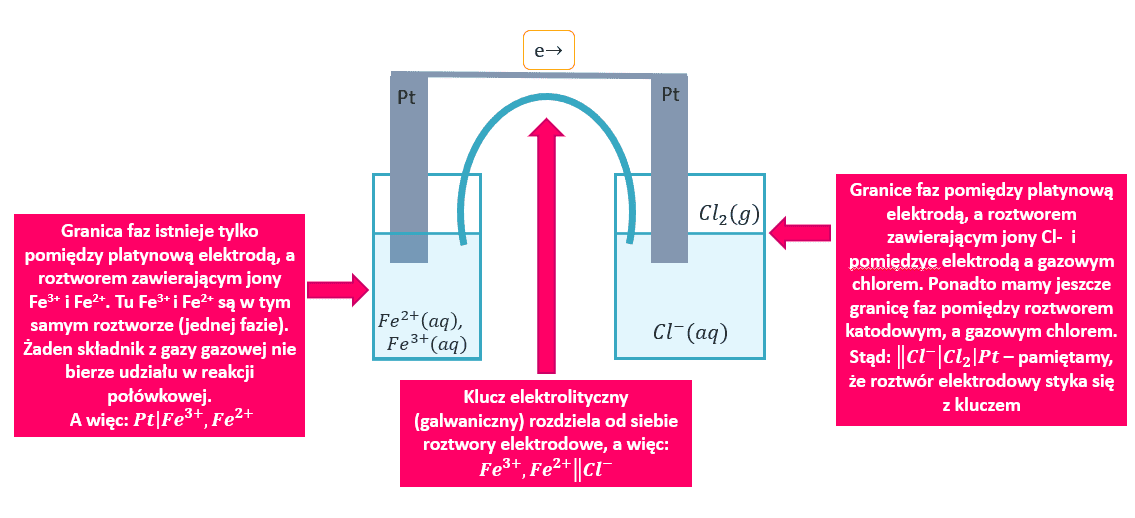
Otrzymujemy zatem:
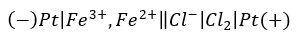
A co w przypadku zadania 12.1 z maja 2024? Spójrzmy do schematu oceniania:
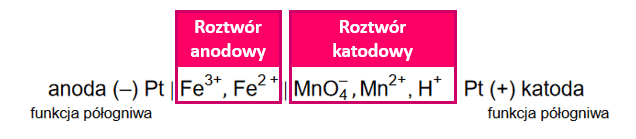
Oznacza to tyle:
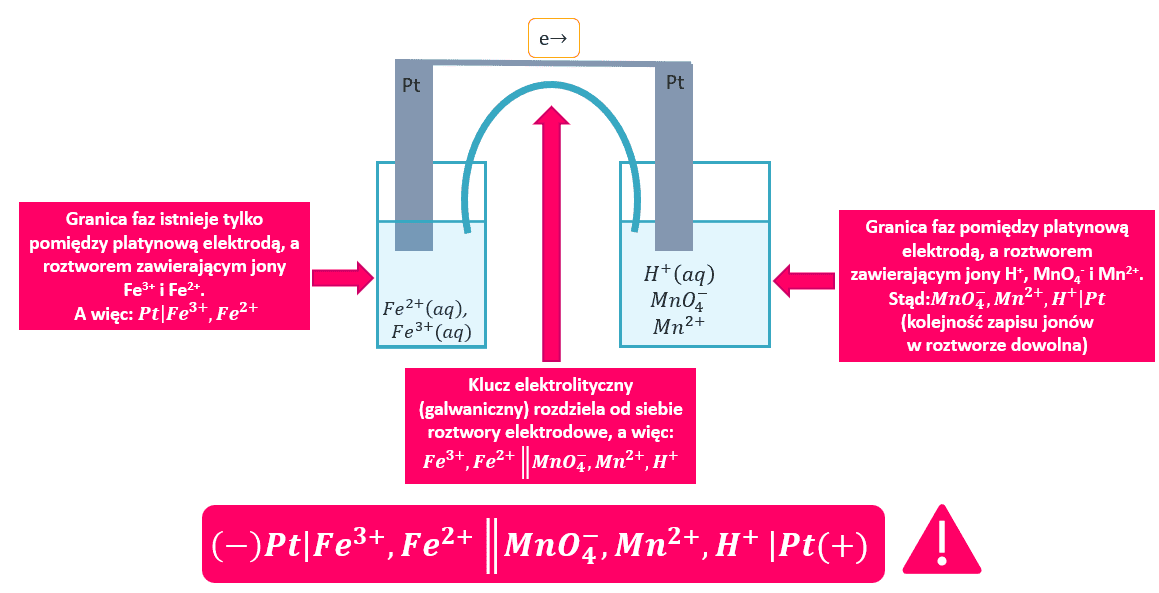
No dobrze, ale jak popatrzymy na zadanie nr 32 z informatora:
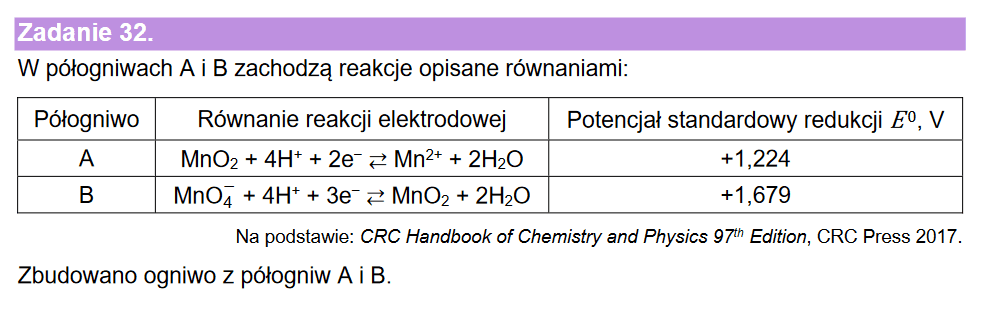
To schemat takiego ogniwa w konwencji sztokholmskiej wygląda następująco:
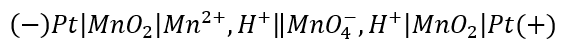
Co wynika stąd, MnO2, jako substancja praktycznie nierozpuszczalna w wodzie - jest osadzona na elektrodzie. I to zarówno na katodzie, jak i na anodzie. W każdym półogniwie mamy więc granice faz: elektroda-MnO2 i MnO2-roztwór elektrodowy. Zarówno na katodzie jak i na anodzie masa MnO2 przyrasta wskutek reakcji synproporcjonowania.
Gdybyśmy w naszym poczciwym ogniwie Daniella:
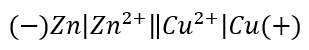
Wymienili katodę na elektrodę chlorosrebrową, to otrzymamy coś takiego:
Czy potraficie już wyjaśnić, dlaczego?
Przejdźmy teraz matury z maja 2025, zadanie 14.


W oficjalnych odpowiedziach widzimy:

Zauważmy, że odpowiedzi raz sugerują, że brom jest rozpuszczony razem z anionami bromkowymy w roztworze anodowym (Br-, Br2), a innym razem mamy pionową kreskę (Br-| Br2), co znaczy, że brom jest w osobnej fazie., że jest w innej fazie niż aniony bromkowe. Brom dość dobrze rozpuszcza się w wodzie, a standardowe potencjały redukcji dotyczą stężenia 1 mol/dm3. Jeśli substancja nie ma na tyle ograniczoną rozpuszczalność, że nie jest w stanie osiągnąć takiego stężenia w 25 °C, to przyjmuje się, że standardowe półogniwo zawiera nasycony roztwór tej substancji, a ponadto układ zawiera tę substancję w osobnej fazie. W przypadku zadania 14.2 takie dopuszczanie obu odpowiedzi wynika to z faktu, że maturzysta nie dostał odpowiednich informacji o tym, czy ten brom jest na tyle dobrze rozpuszczalny w wodzie, by osiągnąć żądane stężenie. Pamiętajmy jednak, że schemat oceniania to nie tylko odpowiedzi poprawne, ale także zakres tolerowanych błędów.
Za taki dopuszczalny błąd należy uznać ten zapis:

Zauważmy, że klucz elektrolityczny powinien się kontaktować z roztworem elektrodowym, np:

Stąd lepsza jest taka kolejność:

Przypadek II - ogniwa bez klucza (mostka) elektrolitycznego.
Jest to przypadek często pomijany w edukacji, a jak pokazuje np. to pytanie:

Powinien być omówiony.
Nie każde ogniwo galwaniczne zawiera mostek solny (klucz elektrolityczny, klucz solny, mostek elektrolityczny). Niektóre zawierają porowatą przegrodę rozdzielającą roztwory elektrodowe, ale jony mogą przez tę przegrodę migrować podobnie jak przez sam klucz (mostek). W schematach taki ogniw przegrodę zaznacza się symbolem pionowej przerywanej kreski (¦).
Trzecią grupę ogniw galwanicznych stanowią takie, w których obie elektrody są zanurzone w tym samym roztworze. Przykładem takiego elektrolitu jest ogniwo Volty, które składa się z elektrody miedzianej i cynkowej zanurzonych w roztworze H2SO4:

Anoda cynkowa się roztwarza, za to na miedzianej katodzie wydziela się wodór. Schemat takiego ogniwa zapiszemy następująco:
(−) Zn | H3O+ | Cu (+)
Przejdźmy teraz do zadania ze zbioru dr B. Pac, którego dotyczy powyższe pytanie z grupy maturalnej. Jedno z poleceń każe zapisać schemat ogniwa galwanicznego.

W odpowiedziach widzimy następującą wersję:

Zwróćmy zatem uwagę na ten fragment:

Oznacza to, że nasze ogniwo galwaniczne wygląda tak:

Alternatywnie odpowiedź możemy zapisać tak (H+ lub H3O+ zamiast HCl):
(-)Ag, AgCl | H+, C6H4O2, C6H6O2 | Pt(+)
Przy okazji zwróćmy uwagę na to zestawienie: Ag, AgCl - przecinek stosujemy wtedy, gdy elektroda jest pokryta warstwą trudnorozpuszczalnej substancji. tutaj jest to warstwa AgCl pokrywajacą srebrną anodę.