
Dziwny peptyd i dziwny aldehyd
Reakcja biuretowa, próba Tollensa czy Trommera to te reakcje, które zna każdy chemik w Polsce. W Polsce, bo poza Centralną Europą raczej mało kto wie o próbie Trommera, która straciła znaczenie w XIX wieku. Ale pozostałe dwie – znają wszyscy chemicy na świecie.
O próbie Trommera uczymy się, że ulegają jej aldehydy. No i to jest prawda - jest to reakcja która pozwala odróżnić na przykład keton od aldehydu. Podobnie rzecz ma się w przypadku próby Tollensa.
A próba biuretowa pozwala nam np. wykryć lub potwierdzić obecność białka w białku jaja kurzego… Albo odróżnić peptyd od np. ketonu. Nazwa tej reakcji pochodzi od biuretu – wizualnie ulega on podobnej reakcji jak peptydy.
Wróćmy do próby Trommera i Tollensa – ulegają jej aldehydy. Ale ulega jej także kwas askorbinowy i wiele innych substancji organicznych, a także niektóre substancje nieorganiczne.
Kwas mrówkowy jest jedną z substancji, które ulegają próbie Tollensa. A często, choć błędnie, sądzi się także, że ulega próbie Trommera. Ściślej, to próbie Tollensa ulegają mrówczany, a nie sam kwas mrówkowy – w silnie zasadowym środowisku odczynnika Tollensa kwas ulega zobojętnieniu. Ale właściwie, to dlaczego mrówczany redukują odczynnik Tollensa? Spójrzmy na wzór strukturalny kwasu mrówkowego:
Gdyby zapytać o to biolchema, jego nauczyciela chemii czy chemika, to chórem odpowiedzą, że to dlatego, że kwas ten, jako jedyny wśród karboksylowych, posiada ugrupowanie aldehydowe i dlatego zachowuje się jak aldehyd.
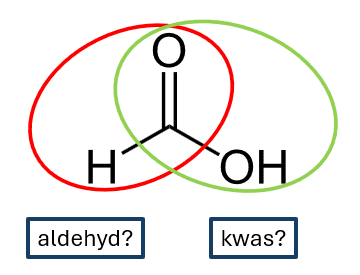
Zastanówmy się najpierw: czy próbie Tollensa lub Trommera ulegają wszystkie aldehydy? Otóż nie… A ponadto niepodobnie do aldehydów to kwas mrówkowy ulega próbie Tollensa, ale Trommera już nie.
Reakcjom tym ulegają te aldehydy, które:
1) Dobrze rozpuszczają się w wodzie
2) Mogą utworzyć formę enolową, np. aldehyd octowy:
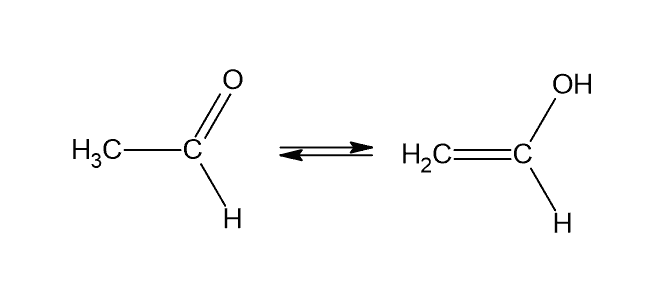
Dlatego reakcjom tym ulega np. etanal, ale już aldehyd benzoesowy albo nawet kwas glioksalowy – nie ulegają. Bo nie mogą utworzyć formy enolowej.
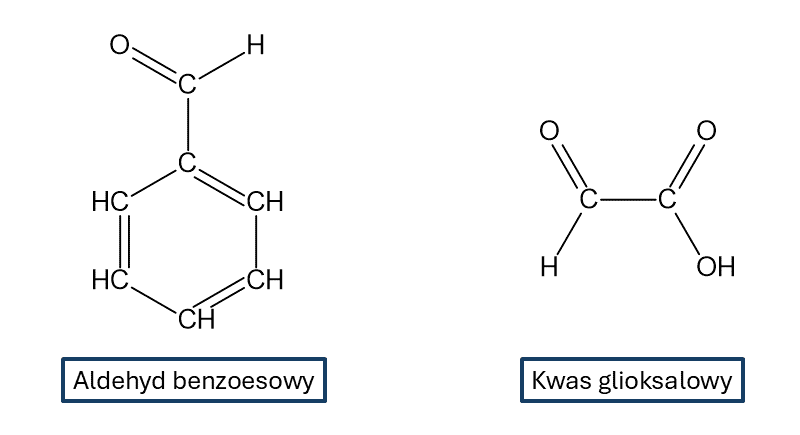
Zwróćmy uwagę, że zarówno aldehyd mrówkowy jak i kwas mrówkowy – nie spełniają drugiego warunku. A mimo to ulegają próbie Tollensa, a aldehyd mrówkowy – także próbie Trommera. Dlaczego tak jest?
Idąc dalej to próbie Trommera i Tollensa ulegają sole kwasu askorbinowego (witaminy C). Spójrzmy na jej wzór półstrukturalny:
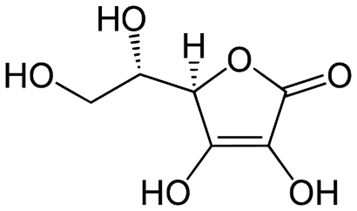
Czy dostrzegamy w nim ugrupowanie aldehydowe -CH=O? Nie… A jednak obserwujemy powstanie ceglastego osadu… Ponadto do znanych reduktorów nieorganicznych należy hydroksyloamina:
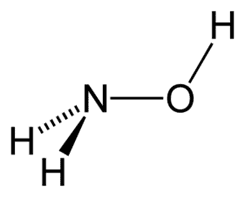
Czy widzimy tutaj ugrupowanie -CH=O? Też nie…
Ustalmy raz na zawsze, że próba Trommera i próba Tollensa nie są reakcjami typowymi dla aldehydów. To są reakcje, które pozwalają odróżnić aldehyd od ketonu (i to też nie zawsze), a nie próby, których pozytywny wynik świadczy o obecności aldehydu.
Alkohole to związki, w których grupa OH związana jest z atomem węgla: C-OH. Ale czy to wystarczające? A może ma jeszcze znaczenie, z czym ten atom węgla jest związany? Jeśli jest związany z atomami wodoru lub grupami alkilowymi/arylowymi – to jest to alkohol:
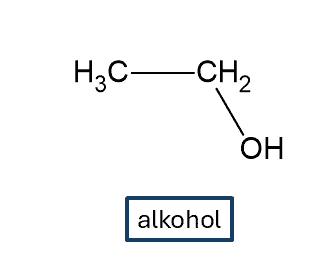
Ale jeśli ten atom węgla związany jest z jeszcze jednym atomem tlenu, to związek przestaje być alkoholem, pomimo, że nadal mamy tam w cząsteczkach grupę OH związaną z atomem węgla:
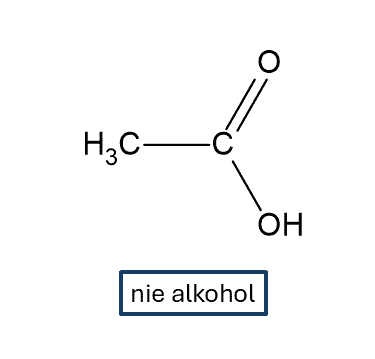
Obecność atomu tlenu zamiast atomów wodoru lub innych atomów węgla związanych z grupą C-OH na tyle zmienia właściwości, że o ile związek o wzorze CH3-CH2-OH zaliczamy do alkoholi, o tyle związek o wzorze CH3CO-OH to kwas karboksylowy. A no właśnie! Trzeba popatrzeć na odpowiednio duży fragment, żeby dojść do poprawnych wniosków. Dlatego CH3-CO-OH to to kwas etanowy, a nie jakiś 1-oksaetanol.
Reakcja jodoformowa to reakcja, której ulegają metyloketony, np. aceton (dimetyloketon), butanon (metyloetyloketon) itp.
I tutaj wiele osób ma zagwozdkę: czy ulega jej kwas octowy? Przecież związek ten ma ugrupowanie CH3CO-. Ale dlaczego mamy się ograniczać do metyloketonów? Reakcji jodoformowej ulegają też metyloalkohole CH3-C-OH. Może więc jest to metyloalkohol?
Tak, cząsteczka kwasu octowego ma ugrupowanie CH3-CO-. Ale ważne jest z czym dalej się to ugrupowanie łączy. Metyloketony to związki o wzorze CH3CO-R. Czym jest R? Atomem wodoru, grupą alkilową lub arylową. Ale nie atomem tlenu. Dlatego CH3-CO-OH to nie jest keton hydroksylo-metylowy, tylko kwas octowy. I nie jest też jakimś metyloalkoholem.
No dobrze, ale co z tym ugrupowaniem aldehydowym w cząsteczce kwasu mrówkowego? No na wzorze go widać przecież. Ale skoro tak, to czy kwas ten (lub jego sole) ulegają reakcjom typowym dla aldehydów? Przecież reakcje aldehydów się na próbie Trommera i Tollensa nie kończą. Kondensacja aldolowa, reakcja Cannizzaro, tworzenie zasad Schiffa, acetalizacja… Czy związek ten ulega którejkolwiek z tych reakcji? Nie… A z aminami tworzy sole lub w odpowiednich warunkach: amidy kwasowe, zamiast zasad Schiffa.
Dlaczego więc ugrupowanie aldehydowe w cząsteczce HCOOH zachowuję się jak aldehydowe w próbie Tollensa, ale w innych reakcjach, którym chętnie ulegają aldehydy, to już nie? Czy argument, że kwas ten zachowuje się zarówno jak kwas karboksylowy lub jak aldehyd ze względu na ugrupowanie jest słuszny?
Zobaczmy, jak wygląda definicja aldehydów na stronie IUPAC: "Compounds RC(=O)H, in which a carbonyl group is bonded to one hydrogen atom and to one R group."
Gdzie przez R rozumiemy atom H, grupę alkilową lub arylową. Grupa –OH nie może być naszym R. Wynika z tego, HCOOH w ogóle nie można rozpatrywać jako aldehydu, a chemiczne właściwości są potwierdzeniem. A że ulega próbie Tollensa – co z tego? To nie jest reakcja zarezerwowana dla aldehydów.
Zresztą zobaczmy na pewną analogię do amin:
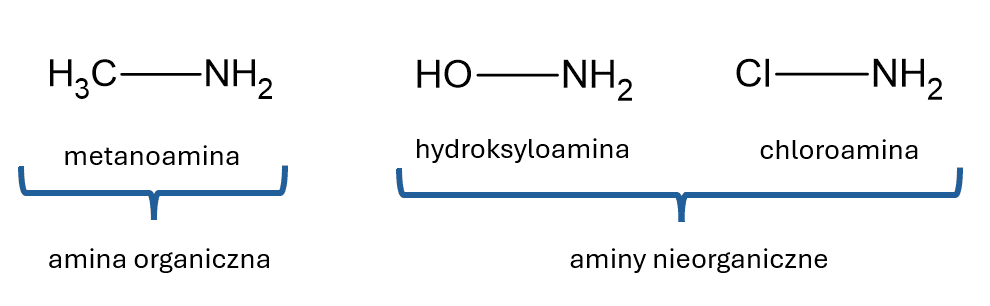
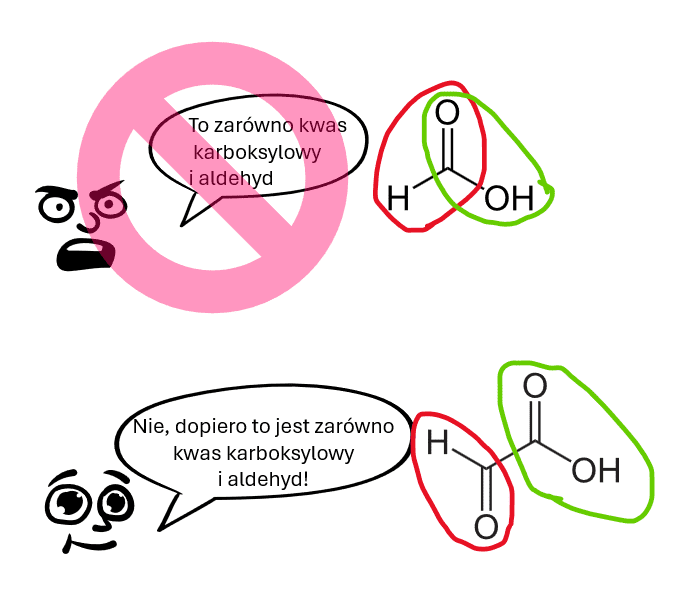
To HCOOH można rozpatrywać jako HOCHO? Hydroksoaldehyd? Aldehyd nieorganiczny? Nieorganiczny, bo grupa CHO nie ma organicznego podstawnika R, tylko grupę OH. Zauważmy, że jak w cząsteczce CH3COOH zamiemimy grupę CH3 na OH, to z cząsteczki kwasu octowego zrobimy cząsteczkę kwasu węglowego. Z cząsteczki związku organicznego zrobimy cząsteczkę związku nieorganicznego… A czy ktokolwiek HCOOH nazywa hydroksoaldehydem? Na szczęście nie. Uświadommy to sobie raz na zawsze: kwas mrówkowy nie jest związkiem dwufunkcyjnym! Ma tylko grupę karboksylową! Nie ma ugrupowania aldehydowego – nie można go rozpatrywać jako kwas i aldehyd równocześnie, bo kluczowa jest grupa OH, która nam grupę CHO zamienia na COOH jako właściwą (i jedyną) grupę funkcyjną. Najprostszym związkiem, który jest i kwasem karboksylowym i aldehydem równocześnie jest kwas glioksalowy (poniżej).
Czy to, że taki benzaldehyd nie ulega próbom Trommera i Tollensa oznacza, że związek ten nie jest aldehydem, bo im nie ulega? Czy to, że kwas askorbinowy (ściślej: askorbiniany) ulega obu próbom czyni aldehyd z witaminy C?
2xNIE.
To teraz zajmijmy się reakcją biuretową. Mało kto ma świadomość, że reakcję tę odkrył polski fizjolog Gustaw Piotrowski (1833 – 1884), pochodzący z Tarnowa. Druga nazwa tej reakcji, a mało rozpowszechniona nawet wśród polskich chemików, to reakcja Piotrowskiego lub odczyn Piotrowskiego. Może jest jakaś tablica pamiątkowa w Tarnowie? Nic mi o tym nie wiadomo, ale skoro każdy chemik i biolog na tym świecie zna reakcję biuretową, to może się takowa przyda? Może jego rodzinny dom jeszcze stoi?
W reakcji biuretowej biorą udział te peptydy, w cząsteczkach których znajdują się co najmniej 2 wiązania peptydowe. Podobnej reakcji ze zalkalizowaną zawiesiną Cu(OH)2 jak peptydy ulega biuret.

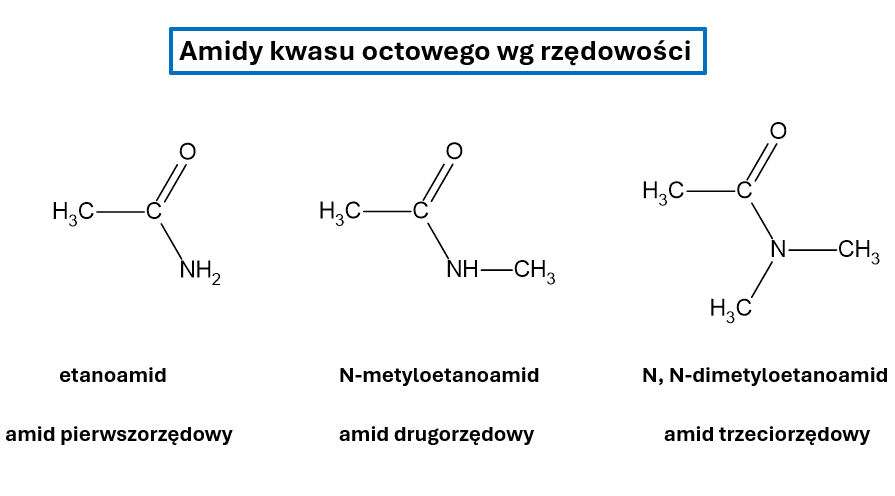
Czymże są peptydy? Są to produkty kondensacji aminokwasów karboksylowych – nie tylko tych białkowych. Od strony chemicznej peptydy są drugorzędowymi amidami.
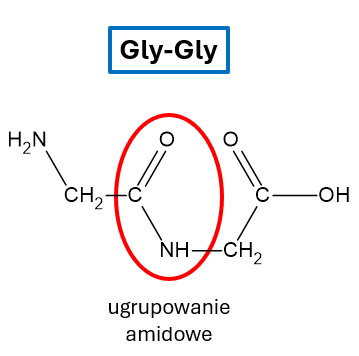
Ugrupowanie peptydowe jest więc drugorzędowym ugrupowaniem amidowym, jak widzimy na przykładzie glicyloglicyny:
A czymże wobec tego jest biuret? Jego nazwa nawiązuje do tego, że można go otrzymać w wyniku kondensacji mocznika – biurea tłumaczone wprost oznacza dwumocznik. Mocznik jest diamidem kwasu węglowego, a biuret?
Teraz wróćmy do tego, że biuret ulega reakcji (nomen omen) biuretowej. W końcu to od niego wzięła się nazwa tej reakcji. Gdyby zapytać biolchema: „Dlaczego biuret ulega reakcji biuretowej?” To usłyszymy odpowiedź, że w cząsteczce jest wiązanie peptydowe. Mówią zresztą o tym same wymagania egzaminacyjne, i to zarówno w formule 2023:

Jak i w formule 2015:

A potem widzimy takie zadania:

I takie odpowiedzi do nich:
No dobrze, ale reakcji biuretowej ulegają te peptydy, które posiadają w swoich cząsteczkach przynajmniej dwa wiązania peptydowe. To niektórzy je próbują znaleźć…
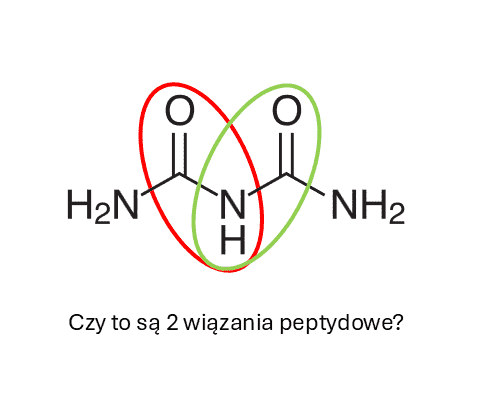
Również pewne zadanie 36 z maja 2017 sugeruje obecność wiązań peptydowych (bo mamy tam liczbę mnogą).

Skoro tak, to ja sobie znajdę wiązania estrowe tutaj. No i co mi kto zrobi?
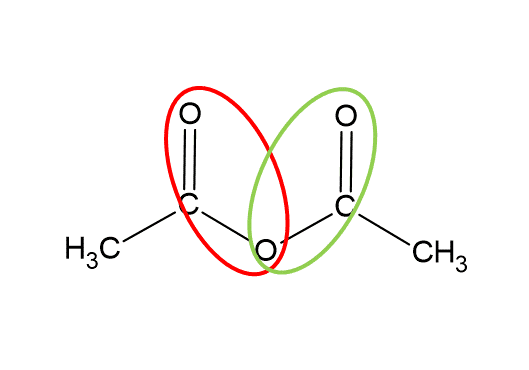
Ale przecież to nie jest ester tylko bezwodnik octowy! To jakim cudem ma tam być wiązanie estrowe?! No właśnie! One są tak samo estrowe, jak to zaznaczone w cząsteczce biuretu są wiązaniami peptydowymi. Wracamy do początku: aby poprawnie określić ugrupowanie funkcyjne trzeba popatrzeć na odpowiednio szerokie połączenie atomów.
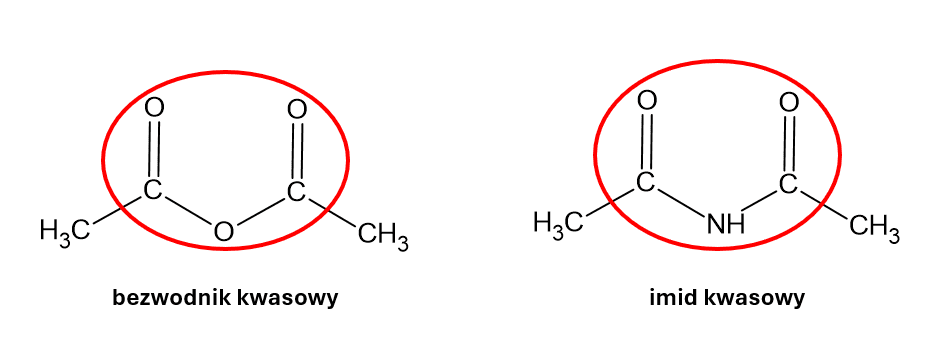
Tak więc dopiero patrząc odpowiednio widzimy, że to nie są dwa ugrupowania estrowe. Ani nawet jedno estrowe. Tylko ugrupowanie bezwodnikowe. Analogicznie, w cząsteczce biuretu mamy ugrupowanie imidowe. Zamiana atomów wodoru na atom tlenu czyni bardzo dużą różnicę…
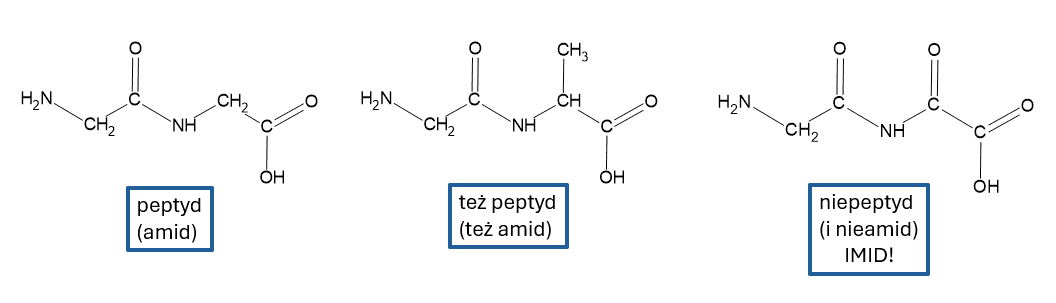
Teraz powiedzcie mi: co się dzieje jak to z alkalizowanej zawiesiny Cu(OH)2 wprowadzimy np glukozę? Zaobserwujemy powstawanie szafirowego roztworu. Ale wręcz identyczną reakcję zaobserwujemy gdy zamiast glukozy użyć np. glicyny. A nawet amoniaku. Że o organicznych aminach już nie wspomnę. I pewnie jeszcze by się wiele znalazło. Czy wobec tego będziemy udowadniać, że glicyna jest diolem? No chyba nie… Bo miałoby to taki sam sens, jak udowadnianie, że witamina C jest aldehydem.
A gdyby ktoś reakcje tworzenia szafirowych roztworów kompleksów Cu(OH)2 nazwał reakcją glicynową? To będziemy udowadniać, że glukoza ma jakieś ugrupowanie aminokwasowe? No dobra, jakieś tam ma… Cząsteczki obu związków mają grupę OH… Jak odpowiednio popatrzeć.
A co z reakcją Piotrowskiego? No ktoś ją kiedyś (może sam Piotrowski?) nazwał reakcją biuretową. Ale czy nie lepiej byłoby ją nazywać tą reakcją Piotrowskiego? Tak jak próba Trommera to nie próba glukozowa, choć została opracowana do wykrywania glukozy w… moczu.
Ludzie! Redukcję związków Cu(II) do ceglastego Cu2O powodują nie tylko aldehydy! Szafirowe kompleksy ze zalkalizowaną zawiesiną Cu(OH)2 tworzą nie tylko związki z ugrupowaniem 1,2-diolowym. A różowofioletowe czy czerwonawe kompleksy ze zalkalizowaną zawiesiną Cu(OH)2 tworzą nie tylko peptydy.
Jeśli w reakcji Piotrowskiego użyć jakiegoś białka, to zajdzie reakcja z wiązaniami (ugrupowaniami) peptydowymi. Ale pikanterii sprawie dodaje fakt, że w reakcji biuretu ze zalkalizowaną zawiesiną Cu(OH)2 w stosunku molowym 2:1 powstaje czerwony związek kompleksowy, którego anion widzimy poniżej*.
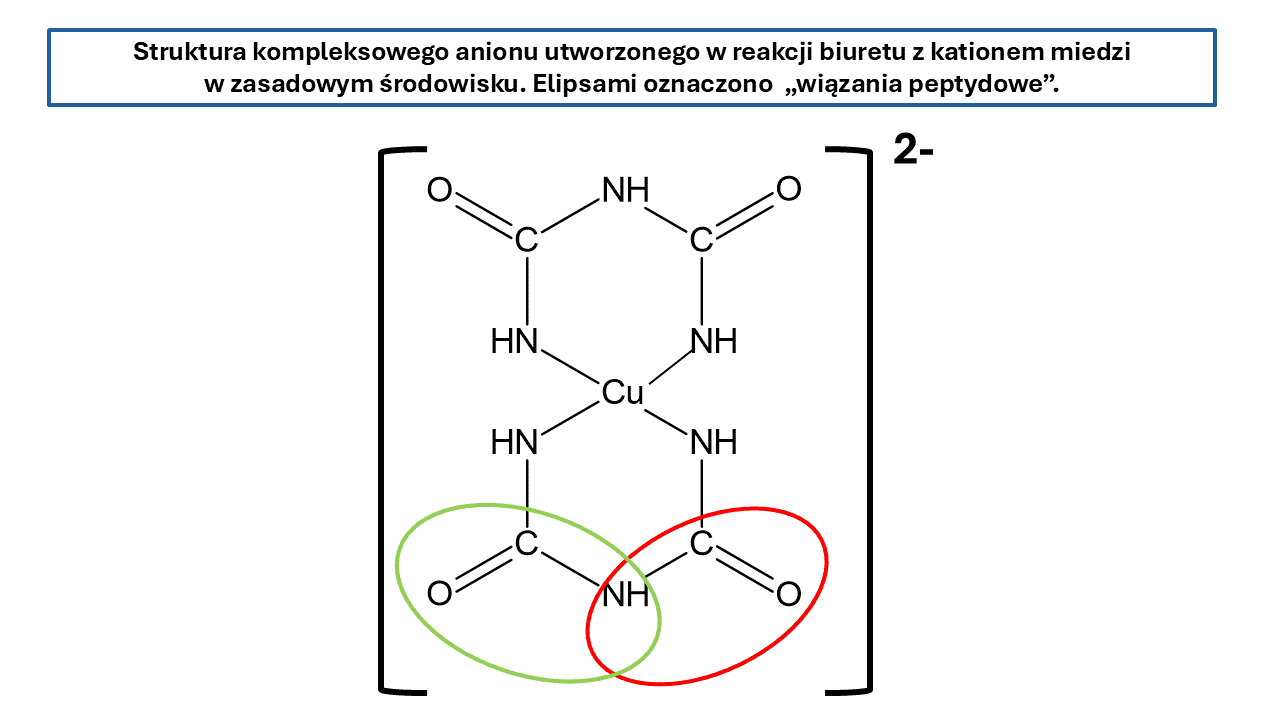
Czy widzimy, że w tworzeniu tego kompleksu nie bierze udziału ani jedno rzekome wiązanie peptydowe? To skrajne grupy NH2 reagują z kationami miedzi! Poza tym, skoro mamy tam dwa „wiązania peptydowe”, to ten jeden atom azotu musiałby tworzyć podwójne wiązanie koordynacyjne do jednego kationu miedzi(II) – a to nawet trudno sobie wyobrazić. No to jak w końcu? Ma dwa wiązania peptydowe, ale nie biorą one udziału w tworzeniu kompleksu? To po co w ogóle miałby być warunek o dwóch wiązaniach peptydowych, skoro on nie biorą one udziału w reakcji? Może i są na tym świecie rzeczy, o których się fizjologom nie śniło, ale nie w tym przypadku…
Ludzie! Nie twórzmy z biuretu peptydu na siłę. Ulega reakcji ze zalkalizowaną zawiesiną Cu(OH)2 no i co z tego? A niech se ulega. Nazwał se to ktoś reakcją biuretową? Nazwał, ale nawet jak nazwę teściową starą kwoką, to nie zacznie znosić złotych jajek. A szkoda. Tak, reakcja Piotrowskiego nie jest ograniczona do wiązań peptydowych, a próby Trommera i Tollensa (2xT) - do grup aldehydowych. Więc można, a raczej powinno się mówić, że reakcji Piotrowskiego ulegają jej peptydy i biuret. A my powtarzamy maniakalnie, że w cząsteczce biuretu są dwa wiązania peptydowe... A co jeśli się okaże, że są związki, które mają jeszcze inną budowę i też ulegają reakcji biuretowej?
Niech cały świat się dowie, że polski fizjolog z Tarnowa w 1857 roku odkrył reakcję, o której do dziś uczą się dzieci na całym świecie! Niech to są rzeczy, o których się będzie fizjologom śniło! Inni się chwalą swoimi osiągnięciami: Trommer, Tollens, Fehling, Kolbe… A niechaj narodowie wżdy postronni znają, iż Polacy nie gęsi, iż swoich fizjologów mają!

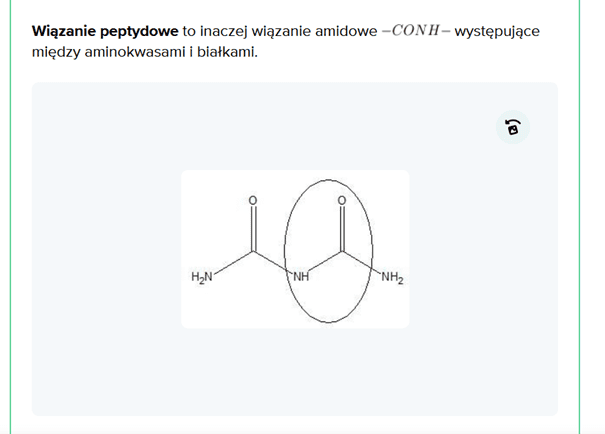
Zmieńmy tę nazwę choćby z tego powodu, żeby nie szerzyć herezji, że biuret to peptyd. Bo tak w praktyce wychodzi. Bo zobaczmy: ma ugrupowanie peptydowe ale nie jest peptydem? To tak, jakby powiedzieć, że ma cząsteczka octanu etylu ma ugrupowanie estrowe, ale to nie czyni jej estrem. A przede wszystkim - przestańmy błędnie używać terminu "wiązanie" w stosunku do grup funkcyjnych. Właściwie –CONH– to nie jest wiązanie peptydowe, tylko ugrupowanie peptydowe, bo przecież to jest grupa funkcyjna, a nie wiązanie. Termin wiązanie jest zarezerwowany dla pary elektronowej. Tak samo –COO– to nie wiązanie estrowe, tylko grupa estrowa. Skoro byłoby to wiązanie, to jaką grupę funkcyjną miałyby mieć estry? Termin wiązanie peptydowe wg IUPAC to wiązanie C-N w grupie –CONH–, a wiązanie estrowe to wiązanie C–O w grupie –COO–.
* Przy stosunku molowym 1:1 otrzymuje się kompleksy o barwie fioletowej („Infrared Spectra and the Structure of Copper Biuret Complexes”, K. Aida, Y. Musya, S. Kinumaki; Inorganic Chemistr, 1963, wol. 2, nr 6, str. 1268-69)
PS